题目内容
在0.1 mol/L的NaHSO3溶液中有如下关系:c(Na+)>c(HSO3-) >c(SO32-) >c(H2SO3),向NaHSO3溶液中慢慢地加入少量的NaOH溶液,发生的主要反应的离子方程式为
A.SO32-+H2O HSO3-十OH— HSO3-十OH— | B.HSO3-十H2O H2SO3十OH- H2SO3十OH- |
C.HSO3-十OH— SO32—十H2O SO32—十H2O | D.H2SO3+OH- HSO3-十H2O HSO3-十H2O |
C
试题分析:NaHSO3溶液中粒子关系为:c(Na+)>c(HSO3-)>c(SO32-)>c(H2SO3),则HSO3-电离大于其水解,溶液显酸性,加入少量的NaOH溶液,发生中和反应,发生的离子反应为HSO3-+OH-=SO32-+H2O,答案选C。

练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目

 2CrO42-+2H+,请写出该平衡的平衡常数表达式K= ,若继续加水稀释,平衡将 移动(填“正向”、“逆向”“不”)。
2CrO42-+2H+,请写出该平衡的平衡常数表达式K= ,若继续加水稀释,平衡将 移动(填“正向”、“逆向”“不”)。
 +4
+4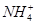

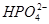 +H2O
+H2O
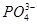 +H3O+
+H3O+