��Ŀ����
�������Ļ�����Ӧ�ù㷺����FeCl3������ӡˢ��·ͭ�帯ʴ����
(1)д��FeCl3��Һ��ʴӡˢ��·ͭ������ӷ���ʽ________��
��ʴͭ���Ļ����Һ�У���Cu2+��Fe3+��Ũ�Ⱦ�Ϊ0.10 mol��L��1����������Һ����ı仯����ԭFeCl2��Һ��Ũ��Ϊ________��
(2)ij��ѧС����ʵ���Ұ������в������븯ʴͭ���Ļ��Һ����ȡ�й����ʣ�ͼʾ���£�
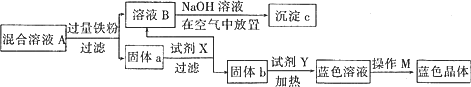
��ش��������⣺
���Լ�XΪ________���Լ�YΪ________������MΪ________��
�ڹ���c�Ļ�ѧʽΪ________��
�ۼ�������ҺB���Ƿ��Fe3+�IJ�����________��
�𰸣�
������
������
|
����(1)2Fe3+��Cu��2Fe2+��Cu2+(2��)��0.3 mol��L��1(1��) ����(2)��ϡ����(1��)��ŨH2SO4(1��)������Ũ������ȴ�ᾧ(���ˡ�ϴ�Ӹ��2��) ������Fe(OH)3(1��) ������ȡ������Һ���Թ��У��ý�ͷ�ιܼ���KSCN��Һ������죮����Fe3+��������Fe3+(2��) |

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ