题目内容
14.铁棒和石墨棒用导线连接后,浸入0.01mol/L 的氯化钠溶液中,下列说法正确的是( )| A. | 铁棒附近产生OH- | B. | 铁棒质量减少 | ||
| C. | 石墨棒上放出氯气 | D. | 石墨棒上放出氧气 |
分析 铁棒与石墨棒用导线连接后浸入0.01mol•L-1的食盐溶液中,构成原电池,Fe为负极,石墨为正极,发生吸氧腐蚀,以此来解答.
解答 解:铁棒与石墨棒用导线连接后浸入0.01mol•L-1的食盐溶液中,构成原电池,Fe为负极,石墨为正极,发生吸氧腐蚀,
A.正极上产生OH-,故A错误;
B.Fe为负极,失去电子而逐渐被腐蚀,故B正确;
C.氯离子不放电,不会产生氯气,故C错误;
D.石墨棒上氧气得电子生成OH-,故D错误;
故选B.
点评 本题考查原电池和吸氧腐蚀,明确电极的判断及发生的电极反应即可解答,题目难度不大.

练习册系列答案
相关题目
4.X、Y、Z、W、M为原子序数依次增大的短周期主族元素.已知①元素对应的原子半径大小为:X<Z<Y<M<W ②原子的最外层电子数:X=W,X+Y=Z=2M ③Y元素的主要化合价:最高正价+最低负价=2,下列说法不正确的是( )
| A. | X、Z两种元素可形成X2Z和X2Z2两种常见共价化合物 | |
| B. | M与Z形成的化合物的分子式为M2Z3 | |
| C. | 工业上可用电解熔融的W的氯化物的方法制取W的单质 | |
| D. | Z元素对应的单质与W元素对应的单质在不同条件下反应产物可能不同 |
19.HPE是合成除草剂的重要中间体,其结构简式如图所示.下列有关HPE的说法正确的是( )
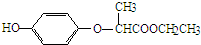
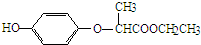
| A. | 含1mol HPE的溶液最多可以和2molNaOH反应 | |
| B. | HPE不能跟浓溴水反应 | |
| C. | 1molHPE能与4molH2发生加成反应 | |
| D. | HPE分子中最多有12个原子共平面 |
6.下列反应的离子方程式正确的是( )
| A. | 把金属铁放入稀硫酸中 2Fe+6H+=2Fe3++3H2↑ | |
| B. | 向Ca(ClO)2溶液中通入二氧化硫 Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO | |
| C. | 向Ca(HCO3)2溶液中加入足量的氢氧化钠溶液 Ca2++HCO3-+OH-=CaCO3↓+H2O | |
| D. | 向NH4HSO4稀溶液中逐滴加入Ba(OH)2溶液至刚好沉淀完全:NH4++H++SO42-+Ba2++2OH-=NH3•H2O+BaSO4↓+H2O |
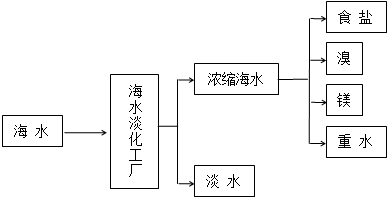
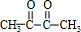
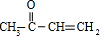 $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$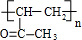
 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$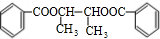 +2H2O.
+2H2O.