��Ŀ����
��ͼ��298K ʱN2��H2��Ӧ�����������仯������ͼ��������������ȷ����
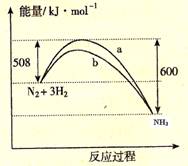
A. �÷�Ӧ���Ȼ�ѧ����ʽΪ��N2(g) +
3H2(g)  2NH3(g), ��H = -92kJ��mol-1
2NH3(g), ��H = -92kJ��mol-1
B. b�����Ǽ������ʱ�������仯����
C. �������, �û�ѧ��Ӧ�Ļ�ܺͷ�Ӧ�ȶ��ı�
D. ���¶����һ����������, ͨ��lmol N2��3molH2 ��Ӧ��ų�������ΪQ1kJ, ��ͨ��2mol N2��6mol H2 ��Ӧ��ų�������ΪQ2kJ ��184>Q2 >2Q1
C
�������������ܸı䷴Ӧ�Ļ�ܣ������ܸı䷴Ӧ�ȣ�����ѡ��C�Ǵ���ģ��������ȷ�ģ���ѡC��

 �����ҵ���������ϵ�д�
�����ҵ���������ϵ�д� �����̸�Ӯ����ٸ�Ч�����ܸ�ϰ���ϿƼ�������ϵ�д�
�����̸�Ӯ����ٸ�Ч�����ܸ�ϰ���ϿƼ�������ϵ�д� �����ҵ�����������ѧ���ӳ�����ϵ�д�
�����ҵ�����������ѧ���ӳ�����ϵ�д���08ɽ��ʡ�������ʼ죩��8�֣�I����1����֪298Kʱ2C��s��+O2��g��=2CO(g) ��H1=��221.01kJ?mol��1
C��s��+O2��g��=CO2(g) ��H2=��393.5kJ?mol��1 ��298KʱCO(g)��O2(g)ȼ������CO2(g) ���Ȼ�ѧ��Ӧ����ʽΪ��________��
��2��һ�����͵�������ȼ�ϵ�ؾ��и߷���Ч�ʶ��������ӡ�����Li2CO3��Na2CO3�������λ����������ʣ�һ��ͨ��CO���壬��һ��ͨ�������CO2�Ļ�����壬�Ƶ�ȼ�ϵ�ء�
�õ�ع���ʱ�ĸ�����ӦʽΪ�� ��
��������CO32�������ʵ����ڹ���ʱ ������������١��������䡱����
|
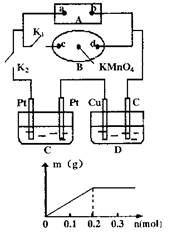
II������ͼ��ʾ��AΪ��Դ��BΪ������ʳ��ˮ�ͷ�̪��Һ����ֽ����ֽ�������һ��KMnO4��Һ��C��D
Ϊ���ۣ���缫���ϼ��������Һ��ͼ��
��1���ر�K1����K2��ͨ���B��KMnO4�Ϻ�ɫҺ����c���ƶ������Դa��Ϊ ����ͨ��һ��ʱ��۲쵽��ֽd�˳��ֵ������ǣ� ��
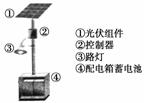
��2����֪Cװ������ҺΪCu(NO3)2��X��NO3��3���Ҿ�Ϊ0.1mol����K1���ر�K2��ͨ��һ��ʱ�������������������m(g)��ͨ�����ӵ����ʵ���n(mol)��ϵ��ͼ��ʾ����Cu2+��X3+��H+���������ɴ�С��˳���� ��Dװ��Cu���ĵ缫��ӦʽΪ ��
 ��1����ͼ��̫���ܵ�ذ徭̫��������ǰ���ڲ����ӵı仯�����ͼ���е��ݱ���������____(��д��N����P��)��������
��1����ͼ��̫���ܵ�ذ徭̫��������ǰ���ڲ����ӵı仯�����ͼ���е��ݱ���������____(��д��N����P��)��������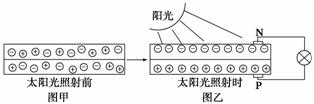
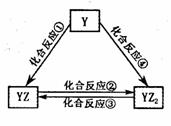 II��X��Y��Z��Q��R5�ֶ�����Ԫ��ԭ���������������������X��Z��Q3��Ԫ����ɣ������£�0.1mol��L-l����Һ��pH =13����ҵ�ϳ��õ��QR������Һ������
II��X��Y��Z��Q��R5�ֶ�����Ԫ��ԭ���������������������X��Z��Q3��Ԫ����ɣ������£�0.1mol��L-l����Һ��pH =13����ҵ�ϳ��õ��QR������Һ������
 2NH3���ǹ�����1905�귢���ģ����˷��ﵽƽ��ʱ��Ӧ���ת���ʲ��ߡ�
2NH3���ǹ�����1905�귢���ģ����˷��ﵽƽ��ʱ��Ӧ���ת���ʲ��ߡ� 2NH3�ķ�Ӧ������ͼ��ʾN2�����ʵ�����ʱ��ı仯���ߡ���H2��ʾ0~10min�ڸ÷�Ӧ��ƽ������v(H2)=_______________����11min��ѹ�����������Ϊ
2NH3�ķ�Ӧ������ͼ��ʾN2�����ʵ�����ʱ��ı仯���ߡ���H2��ʾ0~10min�ڸ÷�Ӧ��ƽ������v(H2)=_______________����11min��ѹ�����������Ϊ