题目内容
已知由短周期元素组成的六种微粒A、B、C、D、E、F其所含原子核数目依次为2、3、4、5、1、1.其中A、B、E各含有18个电子,C、D、F各含有10个电子,A、B、C、D为常见化合物.请回答:
(1)D分子的空间构型为________.
(2)将B缓慢通入Cu(OH)2悬浊液中,浑浊液变为黑色,相应的化学方程式为________.
(3)A、C混合可生成一种新的化合物,该化合物中含有的化学键类型有________;室温下,将pH=a的C的稀溶液与pH=14-a的A稀溶液等体积混合,所得溶液中各离子浓度由大到小的顺序为________.
(4)①若E、F可按1∶1组成离子化合物X,其水溶液呈中性.请写出电解X溶液的化学方程式:________;电解时,阳极收集到的气体体积小于阴极,原因是________.
②若Y溶液中所有离子间有以下关系:c(H+)+3c(F)=c(OH-)+c(E),则:Y溶液的pH________7(填“大于”、“小于”或“等于”),原因是(用离子方程式表示)________.
答案:
解析:
解析:
|
(1)正四面体(1分) (2)H2S+Cu(OH)2=CuS+2H2O(2分) (3)离子键,共价键(2分) c(NH4+)﹥c(Cl-)﹥c(OH-)﹥c(H+)(2分) (4)①2NaCl+2H2O 部分Cl2与NaOH溶液发生了反应而消耗(多答部分Cl2可溶于水不扣分)(2分) (5)小于(1分) Al3++3H2O |

练习册系列答案
 培优三好生系列答案
培优三好生系列答案
相关题目
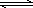 Al(OH)3+3H+(2分)
Al(OH)3+3H+(2分)

