题目内容
已知:H2O(g)===H2O(l) ΔH1=Q1 kJ/mol①
C2H5OH(g)===C2H5OH(l) ΔH2=Q2 kJ/mol②
C2H5OH(g)+3O2(g)===2CO2(g)+3H2O(g) ΔH3=Q3 kJ/mol③
若使1mol乙醇液体完全燃烧,最后恢复到室温,则放出的热量为
C2H5OH(g)===C2H5OH(l) ΔH2=Q2 kJ/mol②
C2H5OH(g)+3O2(g)===2CO2(g)+3H2O(g) ΔH3=Q3 kJ/mol③
若使1mol乙醇液体完全燃烧,最后恢复到室温,则放出的热量为
| A.Q1-3Q2+Q3 | B.3Q1-Q2+Q3 | C.Q1+Q2+Q3 | D.2(Q1+Q2+Q3) |
B
考查反应热的有关计算。根据盖斯定律可知,③-②+3×①即得到反应式C2H5OH(l)+3O2(g)===2CO2(g)+3H2O(l),则该反应的反应热是△H=(3Q1-Q2+Q3)kJ/mol,因此正确的答案选B。

练习册系列答案
 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
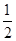 O2(g)===H2O(l) ΔH3=-285.8 kJ/mol
O2(g)===H2O(l) ΔH3=-285.8 kJ/mol
 2NH3(g) ΔH=-92.4 kJ/mol 。在同温同压下向密闭容器中通入1 mol N2和3 mol H2,反应达到平衡时放出热量为Q1 kJ;向另一体积相同的密闭容器中通人0.5 mol N2、1.5 mol H2和1 mol NH3,相同条件下达到平衡时放出热量为Q2 kJ。则下列关系式正确的是
2NH3(g) ΔH=-92.4 kJ/mol 。在同温同压下向密闭容器中通入1 mol N2和3 mol H2,反应达到平衡时放出热量为Q1 kJ;向另一体积相同的密闭容器中通人0.5 mol N2、1.5 mol H2和1 mol NH3,相同条件下达到平衡时放出热量为Q2 kJ。则下列关系式正确的是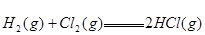 ;
;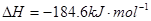 ,则反应
,则反应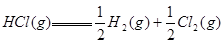 的△H为( )
的△H为( )