题目内容
10.下列各组中属于同位素关系的是( )| A. | 金刚石与石墨 | B. | T2O与H2O | C. | 40K与39K | D. | 16O与16O2- |
分析 A、金刚石与石墨都是碳元素形成的不同的单质;
B、T2O与H2O是化合物;
C、40K和39K为K元素的同位素;
D、16O2-是离子,16O与16O2-的关系为同一种元素形成的不同的微粒.
解答 解:A、金刚石和石墨是碳元素的不同单质,属于同素异形体,故A错误;
B、T2O与H2O是化合物不是元素,所以不是同位素,是同一种物质,故B错误;
C、40K和39K的质子数都是19,40K的中子数是21,39K的中子数是20,所以40K和39K是同位素,故C正确;
D、16O与16O2-的关系为同一种元素形成的不同的微粒,故D错误.
故选C.
点评 本题考查了同位素和同素异形体的判断,侧重于对有关概念的考查,难度不大,注意同位素和同素异形体的区别.

练习册系列答案
相关题目
1.下列说法正确的是( )
| A. | 决定反应速率的因素只有催化剂 | |
| B. | 食物放在冰箱中会减慢食物变质的速率 | |
| C. | 锌与稀硫酸反应时,加入少量水能加快产生氢气的速率 | |
| D. | 增大压强一定能使化学反应速率加快 |
18.下列说法或表示方法中正确的是( )
| A. | 25℃101 kPa时,2C(s)+O2(g)═2CO(g)△H=-221 kJ•mol-1此反应的反应热为221 kJ•mol-1 | |
| B. | 氢气的燃烧热为285.8 kJ•mol-1,则氢气燃烧的热化学方程式为2H2(g)+O2(g)═2H2O(g)△H=-571.6 kJ•mol-1 | |
| C. | 已知2SO2(g)+O2(g)═2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量 | |
| D. | 稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1稀硝酸与稀Ba(OH)2溶液反应的中和热为57.3 kJ•mol-1 |
5.下列叙述中,错误的是( )
| A. | 原子半径:Na>Mg>O | |
| B. | 13C和14C属于同位素 | |
| C. | 0族元素是同周期中非金属性最强的元素 | |
| D. | N和P属于第ⅤA族元素,HNO3酸性比H3PO4的强 |
15.在温度t1和t2下,卤素单质X2(g)和H2反应生成HX学平衡常数如下表所示,仅根据下表数据不能判断的是( )
| 化学方程式 | K(t1) | K(t2) |
| F2+H2?2HF | 1.8×1036 | 1.9×1032 |
| Cl2+H2?2HCl | 9.7×1012 | 4.2×1011 |
| Br2+H2?2HBr | 5.6×107 | 9.3×106 |
| I2+H2?2HI | 43 | 34 |
| A. | 已知t1>t2,HX的生成反应为放热反应 | |
| B. | 在相同条件下,X2平衡转化率a:F2>Cl2 | |
| C. | X2与H2反应的剧烈程度随着原子序数递增逐渐减弱 | |
| D. | HX的稳定性:HBr>HI |
2.已知元素的某种性质“X”和原子半径、金属性、非金属性等一样,也是元素的一种基本性质.下面给出14种元素的X的数值:
试结合元素周期律知识完成下列问题:
(1)根据上表给出的数据,简述主族元素的X的数值大小与元素的金属性或非金属性强弱之间的关系元素X的数值越大,元素的非金属性越强;
(2)简述第二周期元素(除惰性气体外)的X的数值大小与原子半径之间的关系原子半径越小,X的数值越大.
(3)某化合物分子中含有S-N键,你认为该共用电子对偏向于N原子(填元素符号).
(4)经验规律告诉我们:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的化学键一般为离子键;当小于1.7时,一般为共价键.试推断AlBr3中的化学键类型是共价键.
(5)上表中元素形成的AB型化合物中,离子性最强的是NaF.
| 元素 | H | Li | Be | B | C | O | F |
| X的数值 | 2.20 | 0.98 | 1.57 | 2.04 | 2.55 | 3.44 | 3.98 |
| 元素 | Na | Mg | Al | Si | P | S | Cl |
| X的数值 | 0.93 | 1.31 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
(1)根据上表给出的数据,简述主族元素的X的数值大小与元素的金属性或非金属性强弱之间的关系元素X的数值越大,元素的非金属性越强;
(2)简述第二周期元素(除惰性气体外)的X的数值大小与原子半径之间的关系原子半径越小,X的数值越大.
(3)某化合物分子中含有S-N键,你认为该共用电子对偏向于N原子(填元素符号).
(4)经验规律告诉我们:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的化学键一般为离子键;当小于1.7时,一般为共价键.试推断AlBr3中的化学键类型是共价键.
(5)上表中元素形成的AB型化合物中,离子性最强的是NaF.
19. 体育竞技中服用兴奋剂既有失公平,也败坏了体育道德.某种兴奋剂的结构简式如图所示.有关该物质的说法中正确的是( )
体育竞技中服用兴奋剂既有失公平,也败坏了体育道德.某种兴奋剂的结构简式如图所示.有关该物质的说法中正确的是( )
 体育竞技中服用兴奋剂既有失公平,也败坏了体育道德.某种兴奋剂的结构简式如图所示.有关该物质的说法中正确的是( )
体育竞技中服用兴奋剂既有失公平,也败坏了体育道德.某种兴奋剂的结构简式如图所示.有关该物质的说法中正确的是( )| A. | 滴入酸性KMnO4溶液振荡,溶液颜色无变化 | |
| B. | 该物质与苯酚属于同系物 | |
| C. | 1mol该物质和H2反应时最多消耗H26 mol | |
| D. | 1mol该物质与浓溴水反应时最多消Br2 4mol |
20.下列图示与对应的叙述相符的是( )
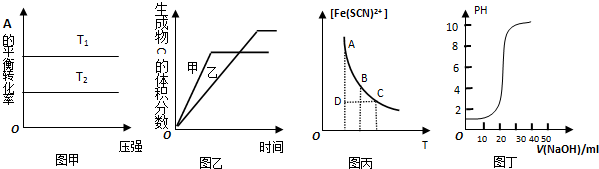

| A. | 由图甲可以判断:对于反应a A (g)+b B (g)?cC (g),若T1>T2,则a+b=c,且△H<0 | |
| B. | 图乙表示温度对可逆反应2A (g)+2 B (g)?3C (g)+D (g)的影响,甲的温度比乙的温度高且正反应为吸热 | |
| C. | 图丙表示可逆反应Fe3+(aq)+SCN-(aq)?Fe(SCN)2+(aq)平衡时,物质的量浓[Fe(SCN)2+]与温度T的关系,反应处于D点时,一定有V(正)>V(逆) | |
| D. | 图丁表示用0.1000mol/L的NaOH溶液滴定20.00ml,0.1000mol/L的醋酸溶液得到的滴定曲线 |
 ;
; ;25℃、101kPa时该气态氢化物热值为5×104kJ•kg-1,则其标准燃烧热为-1300kJ/mol;
;25℃、101kPa时该气态氢化物热值为5×104kJ•kg-1,则其标准燃烧热为-1300kJ/mol;