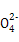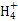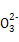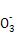МвДҝДЪИЭ
УЙFe2O3ЎўFeЎўCuOЎўCЎўAlЦРөДјёЦЦОпЦКЧйіЙөД»мәП·ЫД©,ИЎСщЖ·ҪшРРПВБРКөСй(Іҝ·ЦІъОпВФИҘ):
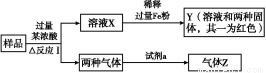
(1)ИЎЙЩБҝИЬТәX,јУИл№эБҝөДNaOHИЬТә,УРіБөнЙъіЙЎЈИЎЙПІгЗеТә,НЁИлCO2,ОЮГчПФұд»Ҝ,ЛөГчСщЖ·ЦРІ»ә¬УРөДОпЦККЗ(МоРҙ»ҜС§КҪ) ЎЈ
(2)ZОӘТ»ЦЦ»тБҪЦЦЖшМе:
ўЩИфZЦ»ОӘТ»ЦЦЖшМе,КФјБaОӘұҘәНNaHCO3ИЬТә,Фт·ҙУҰўсЦРДЬН¬КұЙъіЙБҪЦЦЖшМеөД»ҜС§·ҪіМКҪКЗ ЎЈ
ўЪИфZОӘБҪЦЦЖшМеөД»мәПОп,КФјБaОӘККБҝЛ®,ФтZЦРБҪЦЦЖшМеөД»ҜС§КҪКЗ ЎЈ
(3)ПтYЦРНЁИл№эБҝВИЖш,ІўІ»¶ПҪБ°и,ід·Ц·ҙУҰәу,ИЬТәЦРөДСфАлЧУКЗ(МоРҙАлЧУ·ыәЕ) ЎЈ
(4)ИЎYЦРөДИЬТә,өчpHФјОӘ7,јУИлөн·ЫKIИЬТәәНH2O2,ИЬТәіКПЦА¶Й«ІўУРәмәЦЙ«іБөнЙъіЙЎЈөұПыәД2 mol I-Кұ,№ІЧӘТЖ3 molөзЧУ,ёГ·ҙУҰөДАлЧУ·ҪіМКҪКЗ ЎЈ
(5)БнИЎФӯСщЖ·,јУИлЧгБҝПЎБтЛбід·Ц·ҙУҰЎЈИфИЬТәЦРТ»¶ЁІ»»бІъЙъYЦРөДәмЙ«№ММе,ФтФӯСщЖ·ЦРЛщУРҝЙДЬҙжФЪөДОпЦКЧйәПКЗ(ёчЧйәПЦРөДОпЦКУГ»ҜС§КҪұнКҫ) ЎЈ
(1)Al (2)ўЩC+2H2SO4(ЕЁ) CO2Ўь+2SO2Ўь+2H2O ўЪNOЎўCO2 (3)Cu2+ЎўFe3+ЎўH+ (4)2Fe2++3H2O2+4I-=2Fe(OH)3Ўэ+2I2 (5)CuOЎўC»тCuOЎўCЎўFe2O3
CO2Ўь+2SO2Ўь+2H2O ўЪNOЎўCO2 (3)Cu2+ЎўFe3+ЎўH+ (4)2Fe2++3H2O2+4I-=2Fe(OH)3Ўэ+2I2 (5)CuOЎўC»тCuOЎўCЎўFe2O3
ЎҫҪвОцЎҝҪвМвөД№ШјьИЎҫцУЪЕЁЛб»ҜС§КҪөДЕР¶П,ҪвҙрКұҝЙПИјЩЙиФЩСйЦӨЕЕіэЎЈСщЖ·јУИлДіЕЁЛбәуДЬІъЙъБҪЦЦЖшМе,УЙСщЖ·іЙ·ЦЦӘ,ёГЛбІ»»бКЗСОЛб,ИфОӘСОЛбЦ»ДЬІъЙъH2,№КЕЁЛбОӘЕЁH2SO4»тЕЁHNO3ЎЈ
(1)ИЬТәXјУИл№эБҝNaOHИЬТәәу,Fe3+»тCu2+өИҫщЧӘ»ҜОӘіБөн,ИфУРAl,ФтЧӘ»ҜОӘAlO2-,ВЛТәЦРНЁИлCO2Кұ»бУРAl(OH)3іБөнЙъіЙ,ТтОЮГчПФұд»ҜЛөГчФӯ»мәПОпЦРОЮAlЎЈ
(2)ИфЕЁЛбОӘЕЁH2SO4,ЙъіЙөДБҪЦЦЖшМеЦ»ДЬОӘSO2әНCO2,ИфЕЁЛбОӘЕЁHNO3,ЙъіЙөДБҪЦЦЖшМеОӘNO2әНCO2,ўЩөұНЁИлNaHCO3ИЬТәКұ,ZЦ»ОӘТ»ЦЦЖшМе,ЛөГчФӯЖшМеОӘSO2әНCO2,·ҙУҰўс»ҜС§·ҪіМКҪОӘC+2H2SO4(ЕЁ) CO2Ўь+2SO2Ўь+2H2OЎЈ
CO2Ўь+2SO2Ўь+2H2OЎЈ
ўЪИфНЁ№эЛ®Кұ,ЖшМеZОӘБҪЦЦЖшМе,ЛөГчФӯЖшМеОӘNO2әНCO2,НЁ№эЛ®Кұ·ўЙъ·ҙУҰ:3NO2+H2O=2HNO3+NO,ЛщУаБҪЦЦЖшМеОӘNOәНCO2ЎЈ
(3)УЙСщЖ·өДіЙ·Ц,ҪбәП(1)ЦРЕР¶ПЦӘ,Фӯ»мәПОпЦРОЮAl,јУИл№эБҝМъ·ЫәуYЦРөДҪрКфСфАлЧУЦ»УРFe2+,ІРБф№ММеОӘ№эБҝөДМъәНұ»ЦГ»»іцөДНӯ,өұПтЖдЦРНЁИл№эБҝCl2ІўІ»¶ПҪБ°иәу,Fe2+ЎўFeҫщ»бұ»Сх»ҜОӘFe3+,Cuұ»Сх»ҜОӘCu2+,№КИЬТәЦРҙжФЪөДСфАлЧУУРFe3+ЎўCu2+ЎўH+ЎЈ
(4)ИЬТәіКА¶Й«ЛөГчУРI2ЙъіЙ,ИфЦ»Сх»ҜI-,ПыәД2 mol I-УҰЧӘТЖөзЧУ2 mol,ЛөГч2 mol I-ұ»Сх»ҜКұИФУР1 mol Fe2+ұ»Сх»Ҝ,№К·ҙУҰЦРЖдОпЦКөДБҝЦ®ұИn(I-)ЎГn(Fe2+)=2ЎГ1,УЙҙЛНЖЦӘ·ҙУҰОӘ4I-+2Fe2++3H2O2=2Fe(OH)3Ўэ+2I2ЎЈ
(5)ИфТ»¶ЁІ»ІъЙъYЦРөДәмЙ«№ММе,ЛөГчФӯ»мәП·ЫД©ЦРІ»ДЬә¬УРFe,·сФтөҘЦКМъҝЙДЬ»бәНCu2+ЧчУГЙъіЙCuөҘЦК,№КФӯ»мәПОпҝЙДЬОӘCuOЎўC»тCuOЎўCЎўFe2O3ЎЈ

 іӨҪӯЧчТөұҫН¬ІҪБ·П°ІбПөБРҙр°ё
іӨҪӯЧчТөұҫН¬ІҪБ·П°ІбПөБРҙр°ёёщҫЭПВБРМхјюјЖЛгУР№Ш·ҙУҰөДмКұдЈә
ЈЁ1Ј©ТСЦӘЈәTi(s)Ј«2Cl2(g)=TiCl4(l)ҰӨHЈҪЈӯ804Ј®2 kJЎӨmolЈӯ1
2Na(s)Ј«Cl2(g)=2NaCl(s)ЎЎҰӨHЈҪЈӯ882Ј®0 kJЎӨmolЈӯ1
Na(s)=Na(l)ЎЎҰӨHЈҪЈ«2Ј®6 kJЎӨmolЈӯ1
Фт·ҙУҰTiCl4(l)Ј«4Na(l)=Ti(s)Ј«4NaCl(s)өДҰӨHЈҪ________ kJЎӨmolЈӯ1ЎЈ
ЈЁ2Ј©ТСЦӘПВБР·ҙУҰКэЦөЈә
·ҙУҰРтәЕ | »ҜС§·ҙУҰ | ·ҙУҰИИ |
ўЩ | Fe2O3(s)Ј«3CO(g)= 2Fe(s)Ј«3CO2(g) | ҰӨH1ЈҪЈӯ26Ј®7 kJЎӨmolЈӯ1 |
ўЪ | 3Fe2O3(s)Ј«CO(g)=2Fe3O4(s)Ј«CO2(g) | ҰӨH2ЈҪЈӯ50Ј®8 kJЎӨmolЈӯ |
ўЫ | Fe3O4(s)Ј«CO(g)=3FeO(s)Ј«CO2(g) | ҰӨH3ЈҪЈӯ36Ј®5 kJЎӨmolЈӯ1 |
ўЬ | FeO(s)Ј«CO(g)=Fe(s)Ј«CO2(g) | ҰӨH4 |
Фт·ҙУҰўЬөДҰӨH4ЈҪ____________ kJЎӨmolЈӯ1ЎЈ
AЎўBЎўCИэЦЦЗҝөзҪвЦК,ЛьГЗФЪЛ®ЦРөзАліцөДАлЧУИзПВұнЛщКҫ:
СфАлЧУ | Na+ЎўK+ЎўCu2+ |
ТхАлЧУ | S |
ИзНј1ЛщКҫЧ°ЦГЦР,јЧЎўТТЎўұыИэёцЙХұӯЦРТАҙОКў·ЕЧгБҝөДAИЬТәЎўЧгБҝөДBИЬТәЎўЧгБҝөДCИЬТә,өзј«ҫщОӘКҜД«өзј«ЎЈҪУНЁөзФҙ,ҫӯ№эТ»¶ОКұјдәу,ІвөГТТЦРcөзј«ЦКБҝФцјУБЛ16 gЎЈіЈОВПВёчЙХұӯЦРИЬТәөДpHУлөзҪвКұјдtөД№ШПөИзНј2ЛщКҫЎЈЗл»ШҙрПВБРОКМв:

(1) MОӘЦұБчөзФҙөД ј«,bөзј«ЙП·ўЙъөДөзј«·ҙУҰОӘ ЎЈ
(2)јЖЛгeөзј«ЙПЙъіЙөДЖшМеФЪұкЧјЧҙҝцПВөДМе»эОӘ ЎЈ
(3)РҙіцТТЙХұӯЦРөДЧЬ·ҙУҰөДАлЧУ·ҪіМКҪ: ЎЈ
(4)ТӘК№ұыЙХұӯЦРөДCИЬТә»ЦёҙөҪФӯАҙөДЧҙМ¬,РиТӘҪшРРөДІЩЧчКЗ(РҙіцТӘјУИлөДОпЦКәНЦКБҝ) ЎЈ