题目内容
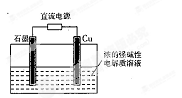
Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如右图所示,电解总反应为:2Cu+H2O Cu2O+H2↑
Cu2O+H2↑
下列说法不正确的是
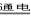 Cu2O+H2↑
Cu2O+H2↑
下列说法不正确的是
| A.石墨电极上产生氢气 |
| B.铜电极发生的电极反应为:2Cu -2e-+2OH-= Cu2O+H2O |
| C.铜电极接直流电源的正极 |
| D.当有0.1 mol电子转移时,有0.1 molCu2O生成 |
D
由电解原理并结合总反应方程式知,Cu做阳极,石墨做阴极,电解的阳极电极
反应式是2Cu-2e-+2OH-=Cu2O+H2O,阴极反应是2H2O-2e-=H2+2OH-。答案选D。
反应式是2Cu-2e-+2OH-=Cu2O+H2O,阴极反应是2H2O-2e-=H2+2OH-。答案选D。

练习册系列答案
相关题目
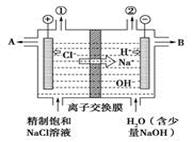
 Cu2O + H2↑。
Cu2O + H2↑。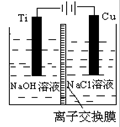
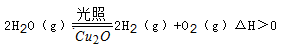
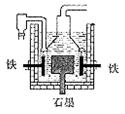
 4Na+2H2O+O2↑。后来盖·吕萨克用铁与熔融 氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH=Fe3O4+4Na↑+2H2↑。下列有关说法不正确的是
4Na+2H2O+O2↑。后来盖·吕萨克用铁与熔融 氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH=Fe3O4+4Na↑+2H2↑。下列有关说法不正确的是