题目内容
1mol白磷转化为红磷时放出18.39kJ热量,已知:P4(白磷,s)+5O2(g)=2P2O5(s) ΔH=-a kJ/mol(a>0);4P(红磷,s)+5O2(g)=2P2O5(s) ΔH=-bkJ/mol(b>0),则a和b的关系是( )
| A.a > b | B.a = b | C.a < b | D.无法确定 |
A
根据盖斯定律可知,①-②即得到P4(白磷,s)=4P(红磷,s),所以反应热ΔH=-a kJ/mol+bkJ/mol=-18.39kJ/mol,所以a大于b,答案选A。

练习册系列答案
相关题目
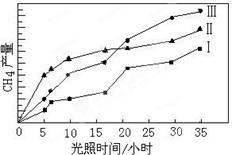
 CO(g)+3H2(g),该反应的ΔH="+206" kJ?mol-1将等物质的量的CH4和H2O(g)充入1L恒容密闭容器,某温度下反应达到平衡,平衡常数K=27,此时测得CO的物质的量为0.10mol,求CH4的平衡转化率(计算结果保留两位有效数字)
CO(g)+3H2(g),该反应的ΔH="+206" kJ?mol-1将等物质的量的CH4和H2O(g)充入1L恒容密闭容器,某温度下反应达到平衡,平衡常数K=27,此时测得CO的物质的量为0.10mol,求CH4的平衡转化率(计算结果保留两位有效数字) CH3OH(g)。
CH3OH(g)。

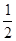 CH4(g)+O2(g)=
CH4(g)+O2(g)= 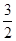 O2(g)=CO(g)+2H2O(1); ?H=-607.3kJ·mol-1
O2(g)=CO(g)+2H2O(1); ?H=-607.3kJ·mol-1