题目内容
已知可逆反应:M(g)+N(g)?P(g)+Q(g);△H>0.在某温度下,反应物的起始浓度分别为:c(M)=1mol/L,c(N)=2.4mol/L,达到平衡时N的转化率为25%.下列说法正确的是( )
分析:M(g)+N(g)?P(g)+Q(g)
起始(mol/L):1 2.4 0 0
转化(mol/L):0.6 0.6 0.6 0.6
平衡(mol/L):0.4 1.8 0.6 0.6
结合外界条件对平衡移动的影响判断平衡移动的方向.
起始(mol/L):1 2.4 0 0
转化(mol/L):0.6 0.6 0.6 0.6
平衡(mol/L):0.4 1.8 0.6 0.6
结合外界条件对平衡移动的影响判断平衡移动的方向.
解答:解:M(g)+N(g)?P(g)+Q(g)
起始(mol/L):1 2.4 0 0
转化(mol/L):0.6 0.6 0.6 0.6
平衡(mol/L):0.4 1.8 0.6 0.6
达到平衡后,M的转化率=
×100%=60%,
A.达到平衡后,M的转化率为60%,故A错误;
B.升高温度,平衡向正反应方向移动,则M的体积分数减小,故B错误;
C.相同条件下,增大N的浓度,反应正向进行,但平衡常数不变,故C错误;
D.相同条件下,若起始时c(M)=c(N),相当于在原来的基础山加入M,则达到平衡后,N的转化率>25%,M和N的转化率相等,则M的转化率>25%,故D正确.
故选D.
起始(mol/L):1 2.4 0 0
转化(mol/L):0.6 0.6 0.6 0.6
平衡(mol/L):0.4 1.8 0.6 0.6
达到平衡后,M的转化率=
| 0.6 |
| 1 |
A.达到平衡后,M的转化率为60%,故A错误;
B.升高温度,平衡向正反应方向移动,则M的体积分数减小,故B错误;
C.相同条件下,增大N的浓度,反应正向进行,但平衡常数不变,故C错误;
D.相同条件下,若起始时c(M)=c(N),相当于在原来的基础山加入M,则达到平衡后,N的转化率>25%,M和N的转化率相等,则M的转化率>25%,故D正确.
故选D.
点评:本题考查化学平衡的计算以及平衡移动问题,题目难度中等,本题易错点为D,注意M和N的物质的量浓度的大小关系对平衡移动的影响.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
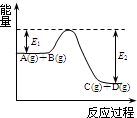 (1)反应A(g)+B(g)
(1)反应A(g)+B(g)  C(g)+D(g)过程中的能量变化如图所示,回答下列问题.
C(g)+D(g)过程中的能量变化如图所示,回答下列问题. P(g)+Q(g)△H>0,请回答下列问题:
P(g)+Q(g)△H>0,请回答下列问题: