题目内容
4.银锌电池广泛用作电子仪器的电源,它的充电和放电过程可表示为:Ag2O+Zn+H2O$?_{充电}^{放电}$2Ag+Zn(OH)2.此电池放电时负极反应的生成物是( )
| A. | Ag | B. | Zn(OH)2 | C. | Ag2O | D. | Zn |
分析 该原电池中,Zn元素化合价由0价变为+2价,则Zn作负极、Ag2O作正极,正极上的反应式为:Ag2O+H2O+2e-=2Ag+2OH-、负极反应式为Zn-2e-+2OH-=Zn(OH)2,据此分析解答.
解答 解:该原电池中,Zn元素化合价由0价变为+2价,则Zn作负极、Ag2O作正极,正极上的反应式为:Ag2O+H2O+2e-=2Ag+2OH-、负极反应式为Zn-2e-+2OH-=Zn(OH)2,所以电池放电时负极反应的生成物是Zn(OH)2,故选B.
点评 本题考查化学电源新型电池,正确判断正负极及正负极发生的反应是解本题关键,难点是电极反应式的书写,题目难度不大.

练习册系列答案
相关题目
14.下表是周期表的一部分,根据A~I在周期表中的位置,用元素符号或化学式回答问题:
(1)表中元素,化学性质最不活泼的是Ar,只有负价而无正价的是F,可用于制半导体材料的元素是Si.
(2)最高价氧化物的水化物碱性最强的物质的电子式是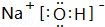 ,酸性最强的物质是HClO4,呈两性的物质是Al(OH)3;
,酸性最强的物质是HClO4,呈两性的物质是Al(OH)3;
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的化合物是HF;
(4)B元素与A形成的化合物和水反应后溶液呈碱性,同时生成一种可燃气体,写出反应的化学方程式NaH+H2O=NaOH+H2↑.
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | |||||
| 3 | B | C | J | F | H | I |
(2)最高价氧化物的水化物碱性最强的物质的电子式是
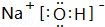 ,酸性最强的物质是HClO4,呈两性的物质是Al(OH)3;
,酸性最强的物质是HClO4,呈两性的物质是Al(OH)3;(3)A分别与D、E、F、G、H形成的化合物中,最稳定的化合物是HF;
(4)B元素与A形成的化合物和水反应后溶液呈碱性,同时生成一种可燃气体,写出反应的化学方程式NaH+H2O=NaOH+H2↑.
12.在2A(g)+B(g)?3C(g)+4D(g)反应中,表示该反应速率最快的是( )
| A. | v(A)=0.5mol•L-1•s-1 | B. | v(B)=0.3 mol•L-1•s-1 | ||
| C. | v(C)=0.6 mol•L-1•s-1 | D. | v(D)=1 mol•L-1•s-1 |
19.与CH2=CH2→CH2Br-CH2Br的变化属于同一反应类型的是( )
| A. | CH3CHO→C2H5OH | B. | C2H5Cl→CH2=CH2 | ||
| C. | C3H7Br→C3H7OH | D. | CH3COOH→CH3COOC2H5 |
9.常温下,能促进水的电离的物质是( )
| A. | 醋酸 | B. | NaOH溶液 | C. | Na2CO3溶液 | D. | 硫酸 |
13.乙醇分子中不同的化学键如图所示,对乙醇在各种反应中应断裂的键说明正确的是( )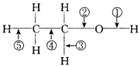

| A. | 和金属钠作用时,键②断裂 | |
| B. | 和浓H2SO4共热至170℃时,键②和⑤断裂 | |
| C. | 在Ag催化剂下和O2反应时,键①和③断裂 | |
| D. | 和CH2COOH共热时,键②断裂 |
14.下列反应的离子方程式中,可以用H++OH-=H2O 表示的是( )
| A. | 醋酸与KOH溶液 | B. | 氢氧化铜与盐酸 | ||
| C. | NaHSO4溶液与氨水 | D. | 硝酸与Ba(OH)2溶液 |
