题目内容
下列有关物质的性质或用途的说法中正确的是
①Cl2具有漂白性,可以直接使有色布条褪色;②SO2具有较强的还原性,不能用浓硫酸干燥;③SiO2是酸性氧化物,能与氢氟酸反应;④Al(OH)3是两性氢氧化物,能溶于强酸或强碱。
| A.①②③ | B.②③④ | C.③④ | D.①②④ |
C
解析试题分析:氯气具有强氧化性,但是不能直接使干燥的有色布条褪色,因此没有漂白性,氯气溶于水时,部分与水反应生成盐酸和次氯酸,由于次氯酸具有漂白性作用,氯气能使湿润的有色布条褪色,故①错;二氧化硫中硫元素为+4价,容易升为+6价,因此具有强还原性,浓硫酸中硫元素为+6价,容易将为+4价,因此具有强氧化性,浓硫酸与二氧化硫不能反应,因为无+5价硫的化合物存在,因此可以用浓硫酸干燥二氧化硫,故②错;二氧化硅与NaOH溶液容易反应,生成硅酸钠和水,但是它不能与盐酸等强酸反应,只能与氢氟酸反应,氢氟酸是弱酸,则二氧化硅是酸性氧化物,故③正确;氢氧化铝与盐酸反应,生成氯化铝和水,氢氧化铝与氢氧化钠反应,生成偏铝酸钠和水,故④正确;综上所述,只有C正确。
考点:考查常见无机物的性质和应用,主要涉及氯气是否具有漂白性、二氧化硫能否用浓硫酸干燥、二氧化硅是否是酸性氧化物、氢氧化铝是否是两性氢氧化物等。

 导学全程练创优训练系列答案
导学全程练创优训练系列答案下列物质转化在给定条件下不能实现的是
| A.①②③ | B.①②④ |
| C.①②③④ | D.①②③④⑤ |
下列物质的转化在给定条件下能实现的是
①氯化钠饱和溶液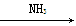
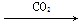 NaHCO3(s)
NaHCO3(s)
②N2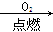 NO2
NO2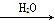 HNO3
HNO3
③海水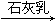 Mg(OH)2
Mg(OH)2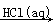 MgCl2(aq)
MgCl2(aq) MgCl2(s)
MgCl2(s)
④Al2O3 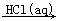 AlCl3(aq)
AlCl3(aq) 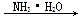 Al(OH)3
Al(OH)3
⑤重晶石(BaSO4) 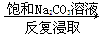 BaCO3
BaCO3 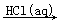 BaCl2(aq)
BaCl2(aq)
| A.①③⑤ | B.②③④ | C.②④⑤ | D.①④⑤ |
根据下列实验现象得出的结论,正确的是
| 选项 | 实验现象 | 结论 |
| A | 某气体能使润湿的淀粉碘化钾试纸变蓝 | 该气体一定是氯气 |
| B | 向某溶液中加入盐酸酸化的BaCl2,有白色沉淀生成 | 该溶液中一定存在SO42- |
| C | 铁与稀硝酸充分反应后,溶液呈浅绿色 | 稀硝酸与铁反应只能生成Fe2+ |
| D | SO2通入溴水中,溴水褪色 | SO2具有还原性 |
从下列事实所得出的相应结论正确的是
| | 实验事实 | 结论 |
| A | 氢氧化铝可以溶解在氢氧化钠溶液中 | 氢氧化铝属于碱 |
| B | CO2的水溶液可导电 | CO2是电解质 |
| C | SO2通入酸性高锰酸钾溶液,溶液褪色 | SO2有漂白性 |
| D | 铁分别和氯气、硫反应得到氯化铁和硫化亚铁 | 氯气的氧化性大于硫 |
下列有关化学反应过程的叙述中,错误的是
| A.船底镶嵌锌块,锌作负极,以防船体被腐蚀 |
| B.除去CO2中的少量SO2:通过盛有饱和NaHCO3溶液的洗气瓶 |
| C.漂白粉和明矾都常用于自来水的处理,二者的作用原理是相同的 |
| D.金属钠在空气中燃烧产生黄色火焰,生成淡黄色固体 |
对下列实验现象的描述不正确的是
| A.光亮的金属Na暴露在空气中,表面逐渐变暗 |
| B.将SO2通入品红溶液,品红溶液褪色 |
| C.将Mg(OH)2固体投入FeCl3溶液中,无明显现象 |
| D.浓硫酸与Cu混合加热,可能有白色固体析出 |
由某金属的混合物(含65%Cu、25%Al、8%Fe及少量Au、Pt)制备硫酸铜和硫酸铝晶体的路线设计如下:
已知物质开始沉淀和沉淀完全时pH如下表:
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Cu(OH)2 |
| 沉淀开始时pH | 2.7 | 4.1 | 8.3 |
| 沉淀完全时pH | 3.7 | 5.4 | 9.8 |
请回答下列问题:
(1)过滤操作用到的玻璃仪器有________。
(2)第①步Al与足量酸反应的离子方程式为___________________________,
得到滤渣1的主要成分为________。
(3)第②步用NaOH调节溶液pH的范围为________。
(4)由第③步得到CuSO4·5H2O晶体的步骤是将滤液2________、________、过滤、洗涤、干燥。
(5)现有洗涤后的滤渣2制取Al2(SO4)3·18H2O,请将a、b、c补充完整。
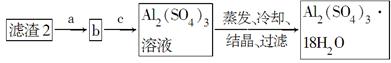

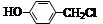 经两步反应制得,写出第一步反应的化学方程式 。
经两步反应制得,写出第一步反应的化学方程式 。