题目内容
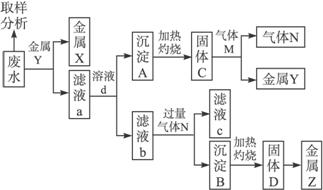
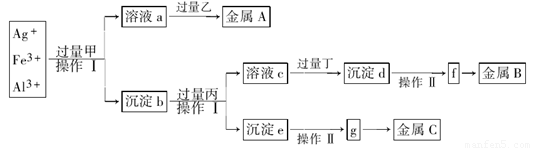
从含有Ag+、Fe3+和Al3+的溶液中,按如图所示方法分离提取金属单质.已知:实验时甲、乙、丙、丁四种物质只能从碳酸铵、氢氧化钠、稀硫酸、葡萄糖四种溶液中选择,也可用这四种溶液来制取.对该实验过程的分析正确的是( )


| A、丙是NaOH,丁是稀H2SO4 | B、乙是葡萄糖,利用乙的还原性将金属A从溶液a中还原出来 | C、操作I是过滤和洗涤沉淀.洗涤沉淀的方法是将漏斗中的沉淀转移到小烧杯中,加蒸馏水浸没沉淀,用玻璃棒搅拌,然后将水倒出,重复2-3次 | D、g是氧化物,金属c采用电解法获得 |
分析:在含有较多Ag+、Fe3+、Al3+的工业废水中加入甲(碳酸铵),Fe3+、Al3+会生成沉淀b(氢氧化铁和氢氧化铝),Ag+反应生成银氨溶液(溶液a),在银氨溶液中加入乙(葡萄糖)会生成金属A(银),沉淀b加入过量的丙(氢氧化钠溶液),氢氧化铝会溶解,过滤后得到沉淀e(氢氧化铁)和溶液c(含偏铝酸钠);氢氧化铁灼烧得到g(氧化铁),氧化铁被还原得到金属C(铁);溶液c加入酸性物质生成氢氧化铝沉淀d,氢氧化铝受热分解得到f氧化铝,电解氧化铝可得金属B(铝).
解答:解:在含有较多Ag+、Fe3+、Al3+的工业废水中加入甲(碳酸铵),Fe3+、Al3+会生成沉淀b(氢氧化铁和氢氧化铝),Ag+反应生成银氨溶液(溶液a),在银氨溶液中加入葡萄糖会生成金属A(银),沉淀b加入过量的氢氧化钠溶液,氢氧化铝会溶解,过滤后得到沉淀e(氢氧化铁)和溶液c(含偏铝酸钠);氢氧化铁灼烧得到g(氧化铁),氧化铁被还原得到金属C(铁);溶液c加入酸性物质生成氢氧化铝沉淀d,氢氧化铝受热分解得到f氧化铝,电解氧化铝可得金属B(铝).
A.丙是NaOH,丁是稀H2SO4,故A正确;
B.银氨溶液中加入葡萄糖会生成单质银,故B正确;
C.洗涤沉淀的方法是向漏斗中加蒸馏水浸没沉淀,待水自然流出后,重复2-3次,不能将沉淀转移到小烧杯中,也不能用玻璃棒搅拌,故C错误;
D.由g(氧化铁)得到金属C(铁)通常用热还原法制得,故D错误;
故选AB.
A.丙是NaOH,丁是稀H2SO4,故A正确;
B.银氨溶液中加入葡萄糖会生成单质银,故B正确;
C.洗涤沉淀的方法是向漏斗中加蒸馏水浸没沉淀,待水自然流出后,重复2-3次,不能将沉淀转移到小烧杯中,也不能用玻璃棒搅拌,故C错误;
D.由g(氧化铁)得到金属C(铁)通常用热还原法制得,故D错误;
故选AB.
点评:本题以从工业废水中分离和提取金属单质为载体,考查了物质的分离提纯方法和原理,把握物质的性质是解题的关键.

练习册系列答案
相关题目
某科研小组从含有较多Ag+、Fe3+、Al3+的工业废水中,按如图所示方法分离和提取金属单质:
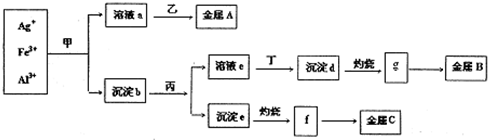
已知:实验室甲、乙、丙、丁四种物质只能从氨水、碳酸铵、氢氧化钠、稀硫酸、葡萄糖五种溶液中选择,也可以用这五种溶液来制备.对该实验分析正确的是( )

已知:实验室甲、乙、丙、丁四种物质只能从氨水、碳酸铵、氢氧化钠、稀硫酸、葡萄糖五种溶液中选择,也可以用这五种溶液来制备.对该实验分析正确的是( )
| A、金属A、B、C分别为Ag、Fe、Al | B、g、f都为氧化物,工业上均采用电解g与f获得对应金属单质 | C、沉淀b为混合物,主要成分为沉淀d和沉淀e | D、甲是氢氧化钠,丁为稀硫酸 |