题目内容
下列叙述正确的是
A.将![]() 通入
通入![]() 溶液中至饱和,无沉淀产生;再通入
溶液中至饱和,无沉淀产生;再通入![]() ,产生沉淀
,产生沉淀
B.在稀硫酸中加入铜粉,铜粉不溶解;再加入![]() 固体,铜粉仍不溶解
固体,铜粉仍不溶解
C.向![]() 溶液中滴加氨水,产生白色沉淀;再加入
溶液中滴加氨水,产生白色沉淀;再加入![]() 溶液,沉淀消失
溶液,沉淀消失
D.纯锌与稀硫酸反应产生氨气的速率较慢;再加入少量![]() 固体,速率不改变
固体,速率不改变
C
解析:本题考查元素及其化合物知识。选项A,CO2、SO2均不能与BaCl2溶液反应,所以再通入SO2时也无沉淀产生。选项B,Cu不能与稀H2SO4反应,但加入Cu(NO3)2后,溶液中存在HNO3,Cu溶解在HNO3中。选项C,Al3+与NH3 ?H2O反应生成Al(OH)3沉淀,加入NaHSO4溶液时,NaHSO4电离出的H+使Al(OH)3溶解。选项D,加入CuSO4溶液后形成原电池而加快了产生H2的速度。

练习册系列答案
相关题目
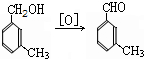
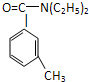 避蚊胺(又名DEET)是一种对人安全、活性高且无抗药性的新型驱蚊剂,其结构简式为:已知:RCOOH
避蚊胺(又名DEET)是一种对人安全、活性高且无抗药性的新型驱蚊剂,其结构简式为:已知:RCOOH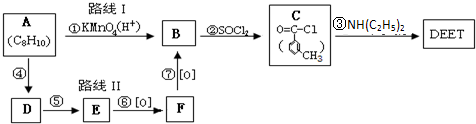
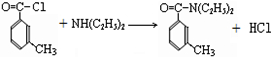
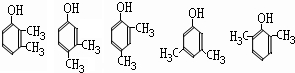 (任写2种)
(任写2种)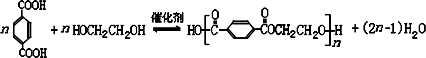
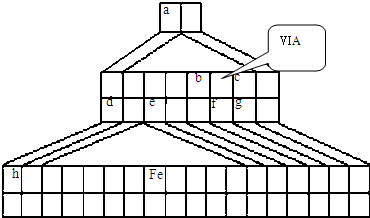
 NH3?H2O+H+
NH3?H2O+H+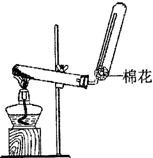 (2010?崇文区二模)X、Y、Z、W均为含有10电子的微粒,其中X、Y、Z为分子,W为离子,且X与Z分子中含有的共用电子对数之比为3:4.
(2010?崇文区二模)X、Y、Z、W均为含有10电子的微粒,其中X、Y、Z为分子,W为离子,且X与Z分子中含有的共用电子对数之比为3:4.