题目内容
在一定条件下,烯烃可发生臭氧氧化还原水解反应,生成羰基化合物,该反应可表示为: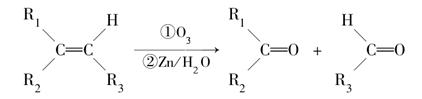
已知:
①化合物A,其分子式为C9H10O,它既能使溴的四氯化碳溶液褪色,又能与FeCl3溶液发生显色反应,且能与金属钠或NaOH溶液反应生成B;
②B发生臭氧氧化还原水解反应生成C,C能发生银镜反应;
③C催化加氢生成D,D在浓硫酸存在下加热生成E;
④E既能使溴的四氯化碳溶液褪色,又能与FeCl3溶液发生显色反应,且能与NaOH溶液反应生成F;
⑤F发生臭氧氧化还原水解反应生成G,G能发生银镜反应,遇酸转化为H(C7H6O2)。
请根据上述信息,写出下列化合物的结构简式(如有多组化合物符合题意,只要求写出其中的一组)。
A:________;C:________;E:________。
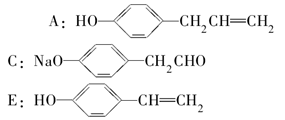
(苯环上的2个基团可以位于邻位或间位)
解析

练习册系列答案
 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
某烃的结构简式为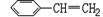 ,它可能具有的性质是 ( )
,它可能具有的性质是 ( )
| A.它能使溴水褪色,但不能使酸性高锰酸钾溶液褪色 |
| B.它既能使溴水褪色,也能使酸性高锰酸钾溶液褪色 |
| C.易溶于水,也易溶于有机溶剂 |
| D.能发生加成反应,一定条件下最多可与三倍物质的量的氢气加成 |
管道煤气的主要成分是CO、H2和少量烃类,天然气的主要成分是CH4,它们燃烧的反应如下:2CO+O2 2CO2,2H2+O2
2CO2,2H2+O2 2H2O,CH4+2O2
2H2O,CH4+2O2 CO2+2H2O,根据以上化学方程式判断:燃烧相同体积的管道煤气和天然气,消耗空气体积较大的是________;因此燃烧管道煤气的灶具如需改用烧天然气,灶具改进的方法是________进风口(填“增大”或“减小”),如不作改进可能产生的不良结果是_____________。
CO2+2H2O,根据以上化学方程式判断:燃烧相同体积的管道煤气和天然气,消耗空气体积较大的是________;因此燃烧管道煤气的灶具如需改用烧天然气,灶具改进的方法是________进风口(填“增大”或“减小”),如不作改进可能产生的不良结果是_____________。
管道煤气中含有的烃类除甲烷外,还有少量乙烷、丙烷、丁烷等,它们的某些性质如下表:
| | 乙烷 | 丙烷 | 丁烷 |
| 沸点(℃) | -88.6 | -42.1 | 0.5 |
试根据以上某个关键数据解释冬天有时管道煤气火焰很小,并且呈断续状态的原因是_____________。
)实验室制备硝基苯的方法是将苯与浓硫酸和浓硝酸的混合液加热到55~60 ℃反应,已知苯与硝基苯的基本物理性质如下表所示:
| | 熔点 | 沸点 | 状态 |
| 苯 | 5.51 ℃ | 80.1 ℃ | 液体 |
| 硝基苯 | 5.7 ℃ | 210.9 ℃ | 液体 |
(1)要配制浓硫酸和浓硝酸的混合酸的注意事项是_________。
(2)分离硝基苯和水的混合物的方法是________;分离硝基苯和苯的方法是__________________________。
(3)某同学用如图装置制取硝基苯:
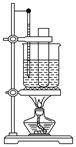
①用水浴加热的优点是_____________________;
②指出该装置的两处缺陷___________________;___________。
 Fe2++SO42-
Fe2++SO42-