题目内容
17.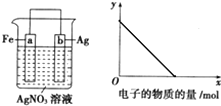 按如图装置进行实验,若x轴表示流入正极的电子的物质的量,则y轴可以表示( )
按如图装置进行实验,若x轴表示流入正极的电子的物质的量,则y轴可以表示( )①c(Ag+) ②c(NO3-) ③a棒的质量 ④b棒的质量 ⑤溶液的质量.
| A. | ①③ | B. | ②④ | C. | ①③⑤ | D. | ②④⑥ |
分析 Fe、Ag、AgNO3构成的原电池中,活泼金属Fe为负极,Ag为正极,Fe和硝酸银之间发生氧化还原反应,在负极上质量减轻,正极上析出金属银.
解答 解:根据图中装置试验,Fe、Ag、AgNO3构成的原电池中,活泼金属Fe为负极,Ag为正极,Fe和硝酸银之间发生氧化还原反应,所以银离子浓度减小,硝酸根浓度不变,故①正确,②错误;
在负极上金属铁本身失电子,即a棒质量减轻,故③正确;
正极Ag上析出金属银,即b棒质量增加,故④错误;
负极上金属铁本身失电子,正极Ag上析出金属银,所以溶液的质量是增加了Fe,但是析出了Ag,但是在转移电子相等情况下,析出金属多,所以溶液质量减轻,但不能为零,故⑤错误;
故选A.
点评 本题考查原电池的工作原理,掌握活泼金属Fe为负极,Ag为正极,Fe和硝酸银之间发生氧化还原反应是解答的关键,题目难度不大.

练习册系列答案
 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目
7.某无色溶液中只可能含有①Na+、②Ba2+、③Cl一、④Br一、⑤SO32一、⑥SO42一离子中的若干种(忽略水电离出的H+、OH-),依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:步骤操作现象
(1)用pH试纸检验溶液的pH大于7
(2)向溶液中滴加氯水,再加入CCl4振荡,静置CCl4层呈橙红色
(3)向所得水溶液中加入Ba(NO3)2溶液和稀HNO3有白色沉淀产生
(4)过滤,向滤液中加入AgNO3溶液和稀HNO3有白色沉淀产生
下列结论正确的是( )
(1)用pH试纸检验溶液的pH大于7
(2)向溶液中滴加氯水,再加入CCl4振荡,静置CCl4层呈橙红色
(3)向所得水溶液中加入Ba(NO3)2溶液和稀HNO3有白色沉淀产生
(4)过滤,向滤液中加入AgNO3溶液和稀HNO3有白色沉淀产生
下列结论正确的是( )
| A. | 肯定含有的离子是③④⑤ | B. | 肯定没有的离子是②⑤ | ||
| C. | 可能含有的离子是①⑥ | D. | 不能确定的离子是③⑥ |
8.下列说法正确的是( )
| A. | 酸和醇反应一定能生成酯,且酯化反应是可逆反应 | |
| B. | 实验证实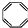 可使Br2/CCl4溶液褪色,说明该分子中存在独立的碳碳单键和碳碳双键 可使Br2/CCl4溶液褪色,说明该分子中存在独立的碳碳单键和碳碳双键 | |
| C. | DDT的结构简式为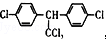 ,分子中最多有14个碳原子共平面 ,分子中最多有14个碳原子共平面 | |
| D. |  的单体是CH3-C≡C-CH3和CH2=CH-CN 的单体是CH3-C≡C-CH3和CH2=CH-CN |
5.某芳香族酯类化合物甲的分子式为C14H10O5,1mol甲水解后只生成一种产物乙,其物质的量为2mol,下列说法正确的是( )
| A. | 符合上述条件的甲共有3种 | |
| B. | 1mol甲最多可以和7molH2发生反应 | |
| C. | 乙中的所有原子一定共平面 | |
| D. | 分别燃烧1mol乙与1mol苯耗氧量相同 |
12.在铜锌原电池中,锌电极上发生的反应为Zn-2e-=Zn2+,则下列说法正确的是( )
| A. | 锌电极为电流流出 | B. | 锌电极为正极 | ||
| C. | 锌电极有气泡 | D. | 反应中Zn被氧化 |
2.化学式为C7H16的烷烃中,在结构式中含有3个甲基的同分异构体数目是( )
| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
9.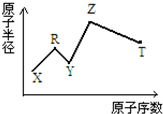 现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T 化合物能破坏水的电离平衡.六种元素的原子半径与原子序数的关系如图所示.下列推断正确的是( )
现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T 化合物能破坏水的电离平衡.六种元素的原子半径与原子序数的关系如图所示.下列推断正确的是( )
 现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T 化合物能破坏水的电离平衡.六种元素的原子半径与原子序数的关系如图所示.下列推断正确的是( )
现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T 化合物能破坏水的电离平衡.六种元素的原子半径与原子序数的关系如图所示.下列推断正确的是( )| A. | 原子半径和离子半径均满足:Y<Z | |
| B. | 氢化物的沸点排序:Y>T>R | |
| C. | 最高价氧化物对应的水化物的酸性:T<R | |
| D. | 由X、R、Y、Z四种元素组成的化合物水溶液一定显酸性 |
6.能说明氯元素的非金属性比硫元素强的事实是( )
| A. | HCl比H2S稳定 | B. | 常温下Cl2为气体,S单质为固体 | ||
| C. | 单质S可以在空气中燃烧Cl2不能 | D. | 溶于水时HCl是强酸而H2S是弱酸 |
7.在下列影响化学反应速率的外界因素中,肯定能使化学反应速率加快的方法是( )
①升高温度 ②加入正催化剂 ③增大反应物浓度 ④将块状固体反应物磨成粉末 ⑤增大压强.
①升高温度 ②加入正催化剂 ③增大反应物浓度 ④将块状固体反应物磨成粉末 ⑤增大压强.
| A. | ①②③④ | B. | ①②④⑤ | C. | ①③④⑤ | D. | ①②③④⑤ |