题目内容
常温下,往 溶液中滴加少量
溶液中滴加少量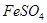 溶液,可发生如下两个反应:
溶液,可发生如下两个反应: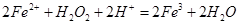 ,
,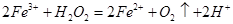 下列说法正确的是
下列说法正确的是
A.在 分解过程中, 分解过程中,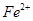 和 和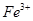 的总量保持不变 的总量保持不变 |
B. 的氧化性比 的氧化性比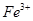 强,其还原性比 强,其还原性比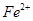 弱 弱 |
C.在 分解过程中,溶液的 分解过程中,溶液的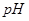 逐渐下降 逐渐下降 |
D. 生产过程中加入少量 生产过程中加入少量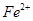 可以提高产率 可以提高产率 |
A
解析试题分析:A、分析题给反应知,Fe3+或Fe2+作H2O2分解的催化剂,所以总量不变,正确;B、由2Fe2++H2O2+2H+=2Fe3++2H2O、2Fe3++H2O2=2Fe2++O2↑+2H+可知,H2O2的氧化性>Fe3+的氧化性,H2O2的还原性>Fe2+的还原性,错误;C、将两个反应相加可得2H2O2=2H2O+O2↑,所以分解过程中,Fe2+作催化剂,溶液pH值不变,错误;D、因为Fe2+可导致H2O2分解,所以H2O2生产过程要避免混入Fe2+,错误。
考点:考查氧化还原反应和催化剂。

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
氰气:(CN)2,结构:N≡C-C≡N;化学性质与卤素单质相似,下列叙述中正确的是
| A.(CN)2分子中C—C键的键长小于F—F键的键长 |
| B.氰化钠和氰化银均不溶于水 |
| C.(CN)2不可以和不饱和烃起加成反应 |
| D.(CN)2和NaOH溶液反应可生成NaCN、NaOCN和H2O |
用氯气消毒的自来水配制下列溶液时,会使配制的溶液变质的是( )
①NaOH ②AgNO3 ③Na2CO3 ④KI ⑤FeCl2
| A.只有②④ | B.只有④⑤ | C.只有②④⑤ | D.全部 |
用图所示装置进行实验,下列对实验现象的解释不合理的是( )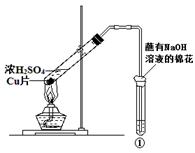
| | ①中试剂 | ①中现象 | 解 释 |
| A | Ba(NO3)2溶液 | 生成白色沉淀 | SO32-与Ba2+生成白色BaSO3沉淀 |
| B | 品红溶液 | 溶液褪色 | SO2具有漂白性 |
| C | 紫色石蕊溶液 | 溶液变红 | SO2与水反应生成酸 |
| D | 酸性KMnO4溶液 | 紫色褪去 | SO2具有还原性 |
欲验证某瓶中装的是氨水,现用一沾有浓盐酸的玻璃棒靠近瓶口,为了使现象明显,可先往瓶中加入一种物质,该物质可以选用下列物质中的( )
①浓H2SO4②固体烧碱③固体碳酸钙④生石灰⑤固体NH4Cl⑥固体食盐
| A.①② | B.②④⑤ | C.②③④⑤ | D.①③⑥ |
下列说法正确的是( )
| A.1 mol Cl2参加反应转移电子数一定为2NA |
| B.在反应KClO3+6HCl=KCl+3Cl2+3H2O中,每生成3 mol Cl2转移电子数为6NA |
| C.SiO2与烧碱反应只生成盐和水,属于酸性氧化物 |
| D.Cl2的水溶液具有酸性,Cl2通入紫色石蕊溶液中,溶液只变红 |
某稀溶液中含4molKNO3和2.5molH2SO4,向其中加入1.5molFe粉,充分反应后产生的NO气体在标准状况下的体积为( )
| A.36L | B.28L | C.22.4L | D.11.2L |
已知硫铁矿在沸腾炉中燃烧,通入的气体原料为空气,其中N2的体积分数为0.8,则沸腾炉中排除的气体中SO2的体积分数可能是( )
| A.0.13 | B.0.16 | C.0.22 | D.0.26 |