题目内容
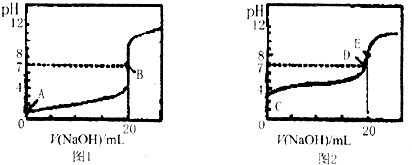
用0.100mol?L-1的硫酸溶液滴定20.0mL0.100mol?L-1的氢氧化钡溶液,并绘制酸碱滴定曲线必须选用的仪器是( )
| A、pH计 | B、胶头滴管 | C、滴定管 | D、量筒 |
分析:pH计可迅速测定溶液的pH,酸碱中和滴定曲线的绘制要使用pH计测定pH,量取硫酸和氢氧化钡反应使用酸式滴定管和碱式滴定管,据此进行判断.
解答:解:A、绘制酸碱滴定曲线,需要测定溶液的pH,pH计可迅速测定溶液的pH,所以必须使用pH计,故A正确;
B、滴定过程中不使用胶头滴管,即胶头滴管不是必须使用的仪器,故B错误;
C、硫酸和氢氧化钡需要使用滴定管,所以滴定管一定会选用,故C正确;
D、滴定操作中不必使用量筒,所以量筒不是必须使用的仪器,故D错误;
故选:AC.
B、滴定过程中不使用胶头滴管,即胶头滴管不是必须使用的仪器,故B错误;
C、硫酸和氢氧化钡需要使用滴定管,所以滴定管一定会选用,故C正确;
D、滴定操作中不必使用量筒,所以量筒不是必须使用的仪器,故D错误;
故选:AC.
点评:本题考查了酸碱中和滴定并绘制酸碱滴定曲线必须选用的仪器,可以根据实验操作选择仪器,本题难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
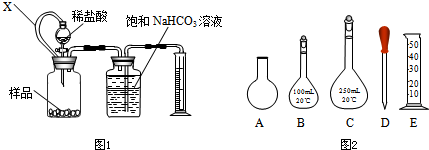
 某化学学习小组借助下列装置(夹持装置已略)及相关试剂粗略测量空气 中O2的体积百分数.
某化学学习小组借助下列装置(夹持装置已略)及相关试剂粗略测量空气 中O2的体积百分数.