题目内容
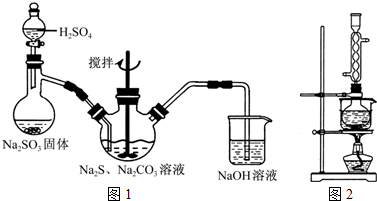
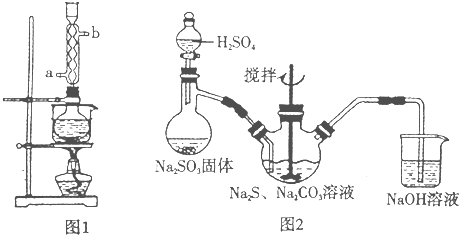
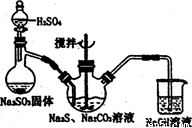
硫代硫酸钠(Na2S2O3)可看成是一个S原子取代了Na2SO4中的一个O原子而形成。某校化学研究性学习小组运用类比学习的思想,通过实验探究Na2S2O3的化学性质。请填写以下空白:
【提出问题】Na2S2O3是否与Na2SO4相似具备下列性质呢?
猜想①:________________________。? ?? 猜想②:溶液呈中性,且不与酸反应。
猜想③:无还原性,不能被氧化剂氧化。
【实验探究】基于上述猜想②、③,设计实验方案。请填写下列表格中的(1)(2)(3)。
| 实验操作 | 实验现象 或预期实验现象 | 现象解释 (用离子方程式表示) |
猜想② |
| 溶液pH约8—10 |
|
向pH=2的硫酸中滴加Na2S2O3溶液 |
| S2O32—+2H+=S↓+SO2↑+H2O | |
猜想③ | 向新制氯水(pH<2)中滴加少量Na2S2O3溶液 | 氯水颜色变浅 |
|
【实验结论】Na2S2O3能与酸反应,具有还原性,与Na2SO4的化学性质不相似。
【问题讨论】
(1)甲同学向探究“猜想③”反应后的溶液中滴加硝酸银溶液,观察到有白色沉淀产生,并据此认为氯水可将Na2S2O3氧化。你认为该方案是否正确并说明理由___________________________________。
(2)请重新设计一个实验方案,证明Na2S2O3被氯水氧化。该实验方案是?????????????????????????????? 。
【提出问题】与BaCl2溶液反应有沉淀生成。
【实验探究】(1)用玻璃棒蘸取Na2S2O3溶液,点滴到pH试纸的中央,半分钟后将试纸呈现的颜色与标准比色卡对照(2)有淡黄色沉淀和无色刺激性气味气体产生。(3) S2O32—+4Cl2+ 5H2O=2SO42—+8Cl— +10H+
【问题讨论】(1)不正确,因氯水过量,氯水中同样含有Cl-。
(2)取少量反应后的溶液,滴加足量的稀盐酸,再向其中滴入氯化钡溶液,若观察到有白色沉淀产生,则说明Na2S2O3能被氯水氧化。
【解析】
试题分析:【提出问题】Na2SO4是强酸强碱盐,能与BaCl2在溶液中发生反应得到既不溶解于水也不溶解于酸的BaSO4沉淀,也无还原性,不能被氧化剂氧化。若Na2S2O3结构与性质和Na2SO4相似,是否也能与BaCl2溶液反应有沉淀生成呢?从而把问题提出来了。
【实验探究】(1)化学实验在验证性质时,如果没有量的要求,试管盖住底部即可。也可以用点滴板等进行,例行节约。若测定溶液的酸碱性,就使用试纸。每次用一条试纸的1/3。用玻璃棒蘸取Na2S2O3溶液,点滴到pH试纸的中央,半分钟后将试纸呈现的颜色与标准比色卡对照,即可确定该溶液的pH。
(2)向pH=2的硫酸中滴加Na2S2O3溶液,发生反应:S2O32—+2H+=S↓+SO2↑+H2O。发生现象:会看到有有淡黄色沉淀产生和放出无色刺激性气味气体。
(3)向新制氯水(pH<2)中滴加少量Na2S2O3溶液,氯水颜色变浅,发生反应:S2O32—+4Cl2+ 5H2O=2SO42—+8Cl—+10H+。证明Na2S2O3有还原性,与Na2SO4的化学性质不相似。
【问题讨论】(1)向探究“猜想③”反应后的溶液中滴加硝酸银溶液,观察到有白色沉淀产生,并据此认为氯水可将Na2S2O3氧化。该方案不正确。因为在氯水中会发生反应:Cl2+H2O=HCl+HClO,氯水本身就含有Cl-。因此不能由此确定该溶液中发生了氧化还原反应。
(2)要证明若Na2S2O3被氧化,则生成了SO42—。只要证明其中含SO42—即可。实验方案是取少量反应后的溶液,滴加足量的稀盐酸,再向其中滴入氯化钡溶液,若观察到有白色沉淀产生,则说明Na2S2O3能被氯水氧化。
考点:考查物质性质的验证、实验方案的设计的知识。