题目内容
(12分)下表是元素周期表的一部分,请回答有关问题:
(1)h元素与k元素形成的化合物的电子式:_____________________;
(2)用电子式表示a与e形成1︰1型化合物的形成过程 。
(3)属于稀有气体的是__________(填元素符号,下同);
(4)第三周期中,原子半径最大的是(稀有气体除外)________________;
(5)推测Si、N最简单氢化物的稳定性__________大于_________(填化学式)。
(6)表中标字母的元素中,能形成两性氢氧化物的元素是________(用元素符号表示,下同),写出该两性氢氧化物与m的氢氧化物的水溶液反应的离子方程式_________;
| | IA | ⅡA | | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 | |
| 1 | a | | b | |||||||
| 2 | | | | | c | d | e | f | g | |
| 3 | h | | I | j | | | k | l | ||
| 4 | m | | | | | | n | | ||
(2)用电子式表示a与e形成1︰1型化合物的形成过程 。
(3)属于稀有气体的是__________(填元素符号,下同);
(4)第三周期中,原子半径最大的是(稀有气体除外)________________;
(5)推测Si、N最简单氢化物的稳定性__________大于_________(填化学式)。
(6)表中标字母的元素中,能形成两性氢氧化物的元素是________(用元素符号表示,下同),写出该两性氢氧化物与m的氢氧化物的水溶液反应的离子方程式_________;
(12分)(1) (2)略 (3) He Ne Ar (4)Na
(2)略 (3) He Ne Ar (4)Na
(5)NH3 > SiH4 (6)Al Al(OH)3+OH-=AlO2-+2H2O
 (2)略 (3) He Ne Ar (4)Na
(2)略 (3) He Ne Ar (4)Na(5)NH3 > SiH4 (6)Al Al(OH)3+OH-=AlO2-+2H2O
a、b、c、d、e、f、g、h、i、j、k、l、m、n对应元素分别为: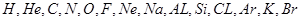 ;
;
(1)h元素与k元素形成的化合物为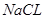 ,电子式为:
,电子式为: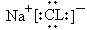 ;
;
(2)a与e形成1︰1型化合物为H2O2,其形成过程为:
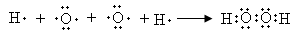
(3)属于稀有气体的是:He Ne Ar
(4)第三周期中,原子半径最大的是(稀有气体除外)Na
(5)推测Si、N最简单氢化物的稳定性NH3 > SiH4;
(6)能形成两性氢氧化物的元素是AL,其对应的碱氢氧化铝与氢氧化钠溶液反应的离子方程式为:Al(OH)3+OH-=AlO2-+2H2O
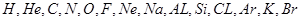 ;
;(1)h元素与k元素形成的化合物为
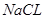 ,电子式为:
,电子式为: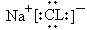 ;
;(2)a与e形成1︰1型化合物为H2O2,其形成过程为:
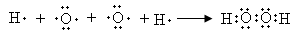
(3)属于稀有气体的是:He Ne Ar
(4)第三周期中,原子半径最大的是(稀有气体除外)Na
(5)推测Si、N最简单氢化物的稳定性NH3 > SiH4;
(6)能形成两性氢氧化物的元素是AL,其对应的碱氢氧化铝与氢氧化钠溶液反应的离子方程式为:Al(OH)3+OH-=AlO2-+2H2O

练习册系列答案
相关题目