题目内容
将30℃时物质A的溶液136g分成两等份,向其中一份中加入10gA,结果只溶解2g就不再溶解;将另一份溶液降温至0℃,析出A5.5g,此时溶质的质量分数为20%,A在30℃时的溶解度为
- A.20g
- B.30g
- C.40g
- D.50g
C

练习册系列答案
相关题目
硫酸亚铁铵的化学式为(NH4)2SO4?FeSO4?6H2O,是浅绿色晶体,商品名为莫尔盐,易溶于水,不溶于乙醇.
完成下面的实验报告:
【实验原理】
【实验用品】
10%Na2CO3溶液、Fe屑、3mol/LH2SO4、(NH4)2SO4固体、蒸馏水、无水乙醇.锥形瓶、蒸发皿、酒精灯、玻璃棒、烧杯、铁架台、漏斗、托盘天平、量筒、滤纸.
【实验步骤】
(1)Fe屑的处理和称量
称取3g铁屑,放入锥形瓶,用l0%Na2CO3溶液,除去Fe屑表面的油污,将剩余的碱液倒掉,用蒸馏水把Fe冲洗干净,干燥后称其质量m1g.
(2)FeSO4的制备
将称量好的Fe屑放人锥形瓶中,加入l5mL 3mol/LH2SO4,加热10min后(有氢气生成,用明火加热注意安全). ,并用少量热水洗涤锥形瓶及滤纸,将滤液和洗涤液一起转移至蒸发皿中.将滤纸上的固体干燥后称得质量为m2g.
①a处的操作是 ;
②制取FeSO4时,加入的Fe为什么要过量?(用离子方程式表示)
(3)(NH4)2SO4?FeSO4?6H2O的制备
根据FeSO4的物质的量,计算并称取(NH4)2SO4固体,并将其加入上面实验的蒸发皿中,缓缓加热,浓缩至表面出现结晶薄膜为止. ,得到硫酸亚铁铵的晶体.过滤后用无水乙醇洗涤晶体,除去其表面的水分,称量得到的晶体质量为m3g.
①b处的操作是 ;②制备莫尔盐晶体时,为什么不能将溶液蒸发至干?
(4)产品检验
微量Fe3+的分析.称0.5g产品置于25mL比色管中,加水溶解后加1mL 25%的KSCN溶液,继续加水至25mL刻度,摇匀,与教师所给标准对比,评价产品质量.写出该过程所发生反应的离子方程式:
【实验记录】
| 温度/℃ 溶解度/g 盐 |
0 | 10 | 20 | 30 | 40 | 50 | 60 |
| (NH4)2SO4 | 70.6 | 73.0 | 75.4 | 78.0 | 81.0 | - | 88.0 |
| FeSO4?7H2O | 15.7 | 20.5 | 26.5 | 32.9 | 40.2 | 48.6 | - |
| (NH4)SO4FeSO4?6H2O | 12.5 | 17.2 | 21.6 | 28.1 | 33.0 | 40.0 | - |
【实验原理】
【实验用品】
10%Na2CO3溶液、Fe屑、3mol/LH2SO4、(NH4)2SO4固体、蒸馏水、无水乙醇.锥形瓶、蒸发皿、酒精灯、玻璃棒、烧杯、铁架台、漏斗、托盘天平、量筒、滤纸.
【实验步骤】
(1)Fe屑的处理和称量
称取3g铁屑,放入锥形瓶,用l0%Na2CO3溶液,除去Fe屑表面的油污,将剩余的碱液倒掉,用蒸馏水把Fe冲洗干净,干燥后称其质量m1g.
(2)FeSO4的制备
将称量好的Fe屑放人锥形瓶中,加入l5mL 3mol/LH2SO4,加热10min后(有氢气生成,用明火加热注意安全).
①a处的操作是
②制取FeSO4时,加入的Fe为什么要过量?(用离子方程式表示)
(3)(NH4)2SO4?FeSO4?6H2O的制备
根据FeSO4的物质的量,计算并称取(NH4)2SO4固体,并将其加入上面实验的蒸发皿中,缓缓加热,浓缩至表面出现结晶薄膜为止.
①b处的操作是
(4)产品检验
微量Fe3+的分析.称0.5g产品置于25mL比色管中,加水溶解后加1mL 25%的KSCN溶液,继续加水至25mL刻度,摇匀,与教师所给标准对比,评价产品质量.写出该过程所发生反应的离子方程式:
【实验记录】
| 起始铁的质量m1/g | 反应后铁的质量m2/g | 莫尔盐的质量 | 产率 | |
| 理论产量/g | 实际产量m3/g | |||
| 5.0 | 2.2 | c | 14.7 | d |
 HCO3-+OH-
HCO3-+OH-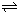 C2D4(g);△H<0.在恒温恒容条件下,将一定量CD2和C2D4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.
C2D4(g);△H<0.在恒温恒容条件下,将一定量CD2和C2D4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.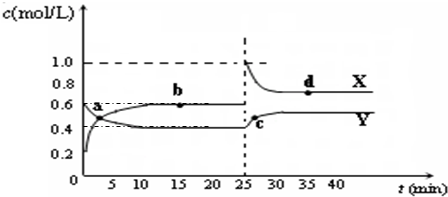
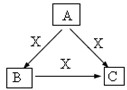 A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图.请针对以下三种不同情况回答:
A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图.请针对以下三种不同情况回答: