题目内容
18.一定质量的铜分别与足量的浓硝酸和稀硝酸完全反应,在相同条件下用排水法收集产生的气体,下列叙述正确的是( )| A. | 硝酸浓度越大,反应消耗的硝酸越少 | |
| B. | 硝酸浓度越大,产生的气体越少 | |
| C. | 硝酸浓度不同,生成Cu(NO3)2的物质的量不同 | |
| D. | 两者用排水法收集到气体体积相等 |
分析 Cu与稀硝酸发生反应:3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O,排水法收集的气体为NO;
Cu与浓硝酸发生反应:Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O、3NO2+H2O═2HNO3+NO,用排水法收集,发生反应:3NO2+H2O═2HNO3+NO,收集的气体为NO,据此进行分析解答.
解答 解:Cu与稀硝酸发生反应:3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O,排水法收集的气体为NO;
Cu与浓硝酸发生反应:Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O、3NO2+H2O═2HNO3+NO,用排水法收集,发生反应:3NO2+H2O═2HNO3+NO,收集的气体为NO,
A.等量的Cu与足量的酸反应,由方程式可知,消耗浓硝酸多,故A错误;
B.等量的Cu与足量的酸反应,浓硝酸反应生成气体多,故B错误;
C.等量的Cu与酸反应,生成Cu(NO3)2的物质的量相同,故C错误;
D.因3NO2+H2O═2HNO3+NO,最终收集气体均为NO,由电子守恒可知,收集NO的体积相等,故D正确;
故选D.
点评 本题考查硝酸性质、化学方程式计算,关键是明确发生的反应,D选项也可以利用关系式判断,题目难度不大.

练习册系列答案
相关题目
8.银耳本身为淡黄色,福建省出产一种雪耳,颜色洁白如雪.其制作过程如下:将银耳堆放在密封状况良好的塑料棚内,在棚的一端置一口锅,锅内放硫磺,加热使硫磺熔化并燃烧,两天左右,雪耳就制成了.这种雪耳是对人体有害的.制作雪耳利用了( )
| A. | 硫的还原性 | B. | 硫的氧化性 | ||
| C. | 二氧化硫的还原性 | D. | 二氧化硫的漂白性 |
9.已知有如下反应:①2BrO3-+Cl2═Br2+2ClO3-,②2FeCl2+Cl2═2FeCl3 ③ClO3-+5Cl-+6H+═3Cl2+3H2O,④2FeCl3+2KI═2FeCl2+2KCl+I2,下列各微粒氧化能力由强到弱的顺序正确的是( )
| A. | ClO3->BrO3->Cl2>Fe3+>I2 | B. | BrO3->Cl 2>ClO3->I2>Fe3+ | ||
| C. | BrO3->ClO3->Cl2>Fe3+>I2 | D. | BrO3->ClO3->Fe3+>Cl2>I2 |
6.已知,向Zn2+离子溶液中滴加氨水,生成Zn(OH)2白色沉淀;但是氨水过量时,沉淀又溶解,生成了Zn(NH3)42+.此外,Zn(OH)2既可溶于盐酸,也可溶于过量NaOH溶液中,生成ZnO22-,所以Zn(OH)2是一种两性氢氧化物.
现有4组离子,每组有2种金属离子.可供选用的试剂有:A硫酸B盐酸 C硝酸 D氢氧化钠溶液 E氨水,选择合适试剂可以让一种离子沉淀一种离子保留在溶液中.
试填空:通过合理选择试剂后将两离子分开后保留在溶液中的离子实际存在形式的符号
现有4组离子,每组有2种金属离子.可供选用的试剂有:A硫酸B盐酸 C硝酸 D氢氧化钠溶液 E氨水,选择合适试剂可以让一种离子沉淀一种离子保留在溶液中.
试填空:通过合理选择试剂后将两离子分开后保留在溶液中的离子实际存在形式的符号
| 离子组 | 保留在溶液中的离子 |
| 1Zn2+和Al3+ | |
| 2Zn2+和Mg2+ | |
| 3Zn2+和Ba2+ | |
| 4Fe3+和Al3+ |
13.下列物质露置在空气中,质量会减轻的是( )
| A. | NaOH | B. | Na2O2 | C. | 浓硫酸 | D. | 浓硝酸 |
3.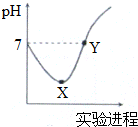 常温下,将Cl2缓慢通入一定量的蒸馏水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol•L-1的NaOH溶液,整个过程中pH变化如图所示,下列叙述正确的是( )
常温下,将Cl2缓慢通入一定量的蒸馏水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol•L-1的NaOH溶液,整个过程中pH变化如图所示,下列叙述正确的是( )
 常温下,将Cl2缓慢通入一定量的蒸馏水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol•L-1的NaOH溶液,整个过程中pH变化如图所示,下列叙述正确的是( )
常温下,将Cl2缓慢通入一定量的蒸馏水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol•L-1的NaOH溶液,整个过程中pH变化如图所示,下列叙述正确的是( )| A. | X、Y两点所示溶液中含有微粒的种类前者多 | |
| B. | X、Y两点所示溶液中水的电离程度前者大 | |
| C. | Y点所示溶液中存在c(Na+)=c(HClO)+2c(ClO-) | |
| D. | X点所示溶液中发生反应的离子方程式为Cl2+H2O═2 H++Cl-+ClO- |
7.下列卤族元素的有关实验,说法正确的是( )
| A. | 往稀米粥中加入少量加碘食盐,能检验食盐中是否含碘 | |
| B. | 已知I3-?I2+I-,向盛有KI3溶液的试管中加人适量CCl4,振荡静置后CCl4层显紫红色,说明KI3在CCl4中的溶解度比在水中的大 | |
| C. | 用溴水即可鉴别苯酚溶液、2,4-己二烯和苯 | |
| D. | 浓盐酸长期暴露在空气中因为见光分解而浓度降低 |
8.Na2FeO4是一种新型水处理剂,可以通过下列反应制取:
湿法制备的主要反应方程为:2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O
干法制备的主要反应方程为:2FeSO4+4Na2O2=2Na2FeO4+2Na2SO4
下列有关该反应的说法错误的是( )
湿法制备的主要反应方程为:2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O
干法制备的主要反应方程为:2FeSO4+4Na2O2=2Na2FeO4+2Na2SO4
下列有关该反应的说法错误的是( )
| A. | 两反应中Na2FeO4均为氧化产物 | |
| B. | Na2FeO4有强氧化性,可消毒杀菌,其还原产物能吸附水中杂质 | |
| C. | 干法中每生成1mol Na2FeO4转移3mol电子 | |
| D. | 碱性条件下,NaClO氧化性大于Na2FeO4 |