题目内容
对于可逆反应N2+3H2?2NH3下列各项所表示的反应速率最快的是( )
| A.V(N2)=0.01mol/(L?S) | B.V(H2)=0.2mol/(L?S) |
| C.V(H2)=0.6mol/(L?S) | D.V(NH3)=1.2mol/(L?S) |
对于反应N2+3H2=2NH3,同一反应中各物质的反应速率之比等于计量数之比,把这些反应速率都换算成H2的反应速率.
A、v(N2)=0.01 mol/(L?s),所以v(H2)=3v(N2)=0.03mol/(L?s);
B、v(H2)=0.2mol/(L?S);
C、v(H2)=0.6mol/(L?S);
D、v(NH3)=1.2mol/(L?s),所以v(H2)=1.5v(NH3)=1.5×1.2mol/(L?s)=1.8mol/(L?S);
故选D.
A、v(N2)=0.01 mol/(L?s),所以v(H2)=3v(N2)=0.03mol/(L?s);
B、v(H2)=0.2mol/(L?S);
C、v(H2)=0.6mol/(L?S);
D、v(NH3)=1.2mol/(L?s),所以v(H2)=1.5v(NH3)=1.5×1.2mol/(L?s)=1.8mol/(L?S);
故选D.

练习册系列答案
相关题目
一定条件下,对于可逆反应N2(g)+3H2(g) 2NH3(g),若N2、H2、NH3的起始浓度分别为C1、C2、C3(均不为零),到达平衡时,N2、H2、NH3的浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.08 mol·L-1,则下列判断正确的是( )
2NH3(g),若N2、H2、NH3的起始浓度分别为C1、C2、C3(均不为零),到达平衡时,N2、H2、NH3的浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.08 mol·L-1,则下列判断正确的是( )
| A.C1:C2=1:3 |
| B.平衡时,H2和NH3的生成速率之比为2:3 |
| C.N2、H2的转化率之比为1:3 |
| D.C1的取值范围为0.04 mol·L-1<C1<0.14 mol·L-1 |
 2NH3(g),若N2、H2、NH3的起始浓度分别为C1、C2、C3(均不为零),到达平衡时,N2、H2、NH3的浓度分别为0.1 mol·L-1、0.3
mol·L-1、0.08 mol·L-1,则下列判断正确的是( )
2NH3(g),若N2、H2、NH3的起始浓度分别为C1、C2、C3(均不为零),到达平衡时,N2、H2、NH3的浓度分别为0.1 mol·L-1、0.3
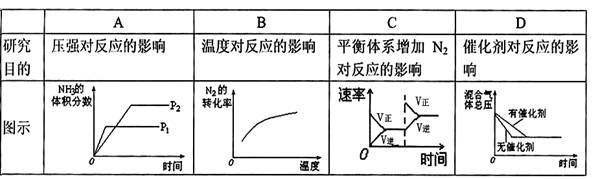
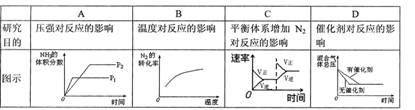
mol·L-1、0.08 mol·L-1,则下列判断正确的是( ) 2NH3(g) △H<0,下列研究目的和图示相符的是
2NH3(g) △H<0,下列研究目的和图示相符的是