题目内容
一定条件下密闭容器中发生如下反应:N2(g)+3H2(g)?2NH3(g),能说明该反应达到化学平衡状态的是( )
分析:反应达到平衡状态时,正逆反应速率相等,平衡时各种物质的物质的量、浓度等不再发生变化,可由此进行判断.
解答:解:A、反应平衡时各物质的浓度是否相等取决于起始时各物质的量的关系和转化的程度,不能作为判断是否达到平衡的依据,故A错误;
B、达到平衡时,正逆反应速率相等,各种物质的浓度不再发生变化,故B正确;
C、该反应为可逆反应,无论是否达到平衡状态,各种物质都共存,故C错误;
D、反应达到平衡时,正逆反应速率相等,但反应并没有停止,故D错误.
故选B.
B、达到平衡时,正逆反应速率相等,各种物质的浓度不再发生变化,故B正确;
C、该反应为可逆反应,无论是否达到平衡状态,各种物质都共存,故C错误;
D、反应达到平衡时,正逆反应速率相等,但反应并没有停止,故D错误.
故选B.
点评:本题考查平衡状态的判断,对于反应前后气体的计量数之和不相等的可逆反应来说,可从浓度、温度、颜色、压强、百分含量等角度判断是否达到平衡状态.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
一定条件下密闭容器中反应2HI(g)═H2(g)+I2(g)达到平衡状态的标志是( )
| A、单位时间内生成n molI2,同时消耗2n molHI | B、单位时间内生成n molI2,同时生成n molHI | C、H2、I2、HI的浓度相等 | D、H2、I2、HI的浓度不随时间变化 |
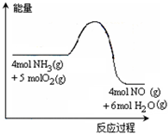 (2010?普陀区二模)一定条件下密闭容器中发生反应:4NH3(g)+5O2(g)
(2010?普陀区二模)一定条件下密闭容器中发生反应:4NH3(g)+5O2(g) 2NH3,下列有关推断正确的是( )
2NH3,下列有关推断正确的是( )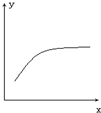 (2011?丰台区二模)一定条件下密闭容器中的可逆反应2A(g)+B(g
(2011?丰台区二模)一定条件下密闭容器中的可逆反应2A(g)+B(g 2C(g),△H<0达到平衡后,改变一个条件x,下列量y的变化一定符合图中曲线的是
2C(g),△H<0达到平衡后,改变一个条件x,下列量y的变化一定符合图中曲线的是