题目内容
2.氢气是清洁能源,也是重要的化工原料.(1)以H2为原料制取氨气进而合成CO(NH2)2的反应如下:
N2(g)+3H2(g)?2NH3(g)△H=-92.40kJ•mol-1
2NH3(g)+CO2(g)?CO(NH2)2(s)+H2O(l)△H=-86.98kJ•mol-1则N2(g)、H2(g)与CO2(g)反应生成CO(NH2)2(s)和H2O(l)的热化学方程式为N2(g)+3H2(g)+CO2(g)=CO(NH2)2(s)+H2O(l)△H=-179.38KJ/mol.
(2)已知H2S高温热分解制H2的反应为H2S(g)?H2(g)+$\frac{1}{2}$S2(g).在体积为2L的恒容密闭容器中,通入3.5molH2S,控制不同温度进行H2S的分解实验,测得H2S的平衡转化率与温度的关系如图1所示.
①985℃时,反应经7min达到平衡,则上述反应从起始至7min内的反应速率v(S2)=0.05mol/(L•min).
②反应S2(g)+2H2(g)?2H2S(g)的△H<(填“>”或“<”)0.
(3)使用石油热裂解的副产物CH4来制取CO和H2,其生产流程如图2所示:
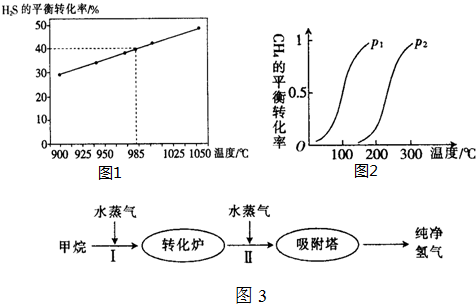
①此流程的第Ⅰ步反应为CH4(g)+H2O(g)?CO(g)+3H2(g),一定条件下CH4的平衡转化率与温度、压强的关系如图3所示.则p1<(填“<”“>”或“=”)p2.
②100℃时,将3mol CH4和4molH2O通入容积为100L的恒容密闭容器中,达到平衡时容器中CO(g)和H2O(g))的浓度相同.100℃时该反应的平衡常数K=0.0216.
分析 (1)N2(g)+3H2(g)=2NH3(g)△H=-92.40kJ•mol-1 ①
2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l)△H=-86.98kJ•mol-1 ②
根据盖斯定律将①+②计算可得;
(2)①根据在985℃时,H2S的转化率为40%,即可求出H2S的物质的量的该变量,然后根据在反应中,物质的量的该变量之比等于计量数之比,即可求出S2的物质的量的该变量,然后根据v=$\frac{\frac{△n}{V}}{△t}$来计算反应速率.
②据图可知,温度越高,H2S的平衡转化率越高,则说明升高温度,反应H2S=H2(g)+$\frac{1}{2}$S2(g)平衡右移,反应吸热,据此判断;
(3)①采取控制变量法分析,由图可知温度相同时,到达平衡时,压强为P1的CH4转化率高,反应为气体体积增大的反应,增大压强平衡向体积减小的方向移动;
②依据化学平衡三段式列式计算平衡浓度结合平衡常数概念计算得到.
解答 解:(1)已知:N2(g)+3H2(g)=2NH3(g)△H=-92.40kJ•mol-1 ①
2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l)△H=-86.98kJ•mol-1 ②
将①+②可得:
N2(g)+3H2(g)+CO2(g)=CO(NH2)2(s)+H2O(l)△H=(-92.4KJ/mol)+(-86.98KJ/mol)=-179.38KJ/mol,
故答案为:N2(g)+3H2(g)+CO2(g)=CO(NH2)2(s)+H2O(l)△H=-179.38KJ/mol.
(2)①在985℃时,H2S的转化率为40%,H2S的物质的量的该变量△n=3.5mol×40%=1.4mol,在反应中,物质的量的该变量之比等于计量数之比,故S2的物质的量的该变量△n=0.7mol,故反应速率v(S2)=v=$\frac{\frac{△n}{V}}{△t}$=$\frac{\frac{0.7mol}{2L}}{7min}$=0.05mol/(L•min),故答案为:0.05mol/(L•min);
②据图可知,温度越高,H2S的平衡转化率越高,则说明升高温度,反应H2S=H2(g)+$\frac{1}{2}$S2(g)平衡右移,反应吸热,故反应S2(g)+2H2(g)=2H2S(g)放热,即△H<0,故答案为:<;
(3)①由图可知温度相同时,到达平衡时,压强为P1的CH4转化率高,平衡向正反应方向移动,反应为气体体积增大的反应,增大压强平衡向体积减小的方向移动,即P1<P2;故答案为:<;
②100℃时,将3mol CH4和4mol H2O通入容积为100L的恒容密闭容器中,CO(g)和H2O(g))的浓度相同,
CH4(g)+H2O(g)?CO(g)+3H2(g)
起始量(mol/L) 0.03 0.04 0 0
变化量(mol/L) 0.02 0.02 0.02 0.06
平衡量(mol/L) 0.01 0.02 0.02 0.06
平衡常数K=$\frac{c(CO)c{\;}^{3}(H{\;}_{2})}{c(CH{\;}_{4})c(H{\;}_{2}O)}$=$\frac{0.02×0.06{\;}^{3}}{0.01×0.02}$=0.0216;
故答案为:0.0216.
点评 本题考查了利用盖斯定律来解题和反应速率的求算、平衡的计算以及利用温度对平衡转化率的影响来分析反应吸热还是放热等,难度不大.

 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案| A. | 1种 | B. | 2种 | C. | 3种 | D. | 5种 |
| A. | 3-氯戊烷的分子式为C5H9Cl3 | B. | 3-氯戊烷属于烷烃 | ||
| C. | 3-氯戊烷能发生取代反应 | D. | 3-氯戊烷的同分异构体共有6种 |
| A. | 镁是第IIA族元素 | |
| B. | 第IA族元素全部是金属元素 | |
| C. | 氧族中含金属元素 | |
| D. | 第3周期中既有金属元素又有非金属元素 |
| A. | 食醋中含有的醋酸 | B. | 酒中含有的酒精 | ||
| C. | 葡萄中含有的葡萄糖 | D. | 谷类中含有的淀粉 |
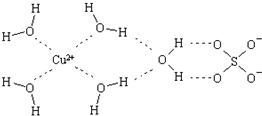 科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如下,其中配位键和氢键均采用虚线表示.
科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如下,其中配位键和氢键均采用虚线表示.