题目内容
10.写出有关化学方程式(1)切开的金属Na暴露在空气中,光亮表面逐渐变暗4Na+O2=2Na2O
(2)苯、浓硝酸、浓硫酸混合加热到55℃左右
 +HNO3(浓)$→_{55℃}^{浓硫酸}$
+HNO3(浓)$→_{55℃}^{浓硫酸}$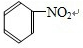 +H2O.
+H2O.
分析 (1)切开的金属Na暴露在空气中,光亮表面逐渐变暗是钠被空气中氧气氧化生成氧化钠;
(2)苯、浓硝酸、浓硫酸混合加热到55℃左右发生取代反应生成硝基苯.
解答 解:(1)切开的金属Na暴露在空气中,光亮表面逐渐变暗是钠被空气中氧气氧化生成氧化钠,反应的化学方程式为:4Na+O2=2Na2O,
故答案为:4Na+O2=2Na2O;
(2)发生取代反应生成硝基苯,反应为 +HNO3(浓)$→_{55℃}^{浓硫酸}$
+HNO3(浓)$→_{55℃}^{浓硫酸}$ +H2O,
+H2O,
故答案为: +HNO3(浓)$→_{55℃}^{浓硫酸}$
+HNO3(浓)$→_{55℃}^{浓硫酸}$ +H2O.
+H2O.
点评 本题考查有机物化学反应方程式的书写,为高频考点,把握常见有机物性质、反应类型、反应条件书写方程式为解答的关键,题目难度不大.

练习册系列答案
相关题目
20.在t℃时,相对分子质量为M的某盐(不含结晶水)的饱和溶液,其物质的量浓度为cmol/L,密度为ρg/cm3,质量分数为a%,溶解度为S g.下列关系式中不正确的是( )
| A. | c=$\frac{ρa%}{M}$ | B. | a%=$\frac{S}{100+S}$×100% | ||
| C. | S=$\frac{Mc}{1000ρ-Mc}$×100 | D. | a%=$\frac{Mc}{1000ρ}$ |
1.下列关于氯的说法正确的是( )
| A. | 氯气具有很强的氧化性,在化学反应中只能作氧化剂 | |
| B. | ${\;}_{17}^{35}$Cl、${\;}_{17}^{37}$Cl为氯元素不同的核素,具有不同的化学性质 | |
| C. | 红热的铜丝在氯气里剧烈燃烧,生成棕黄色的烟雾 | |
| D. | 氯气能与水反应生成次氯酸和盐酸,久置氯水最终变为稀盐酸 |
15.短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13.X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者Y原子最外层电子数的3倍.下列说法正确是( )
| A. | X的氢化物溶于水显酸性 | |
| B. | Z位于周期表的第二周期VIA族 | |
| C. | X和Z的最高价氧化物对应的水化物都是弱酸 | |
| D. | Y的氧化物是离子化合物 |
2.下列关于硅及其化合物的说法中正确的是( )
| A. | 硅是构成一些岩石和矿物的基本元素 | |
| B. | 水泥、玻璃、水晶饰物都是硅酸盐制品 | |
| C. | 高纯度的硅单质广泛用于制作光导纤维 | |
| D. | SiO2既能与酸反应,又能与碱反应,所以它是两性氧化物 |
19.分子式为C5H12O能与金属钠反应放出氢气且可氧化生成醛的有机化合物有(不考虑立体异构)( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
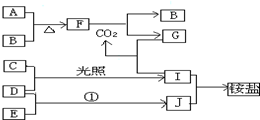
 ;
; 2NH3
2NH3