题目内容
10.a、b、c、d都是短周期元素,原子半径d>c>a>b,其中a、b处在同一周期,a、c处在同一主族.c原子核内质子数等于a、b原子核内质子数之和,c原子最外层上的电子数是d原子次外层电子数的一半.下列说法中正确的( )| A. | a、c两元素处在元素周期表的VIA族 | |
| B. | b、d两种元素可组成化学式为d2b2的化合物,且阴阳离子个数比为1:2 | |
| C. | c单质可在b单质中燃烧生成的化合物的分子式为cb2 | |
| D. | c的单质可用来制作光导纤维 |
分析 a、b、c、d都是短周期元素,原子半径d>c>a>b,其中a、b处在同一周期,a、c处在同一主族,可以判断a、b处于第二周期,c处于第三周期,a、c处在同一主族,二者质子数相差8,c原子核内质子数等于a、b原子核内质子数之和,故b的质子数为8,则b为O元素;c原子最外层上的电子数是d原子次外层电子数的一半,d不能处于第二周期,只能为第三周期元素,故c最外层电子数为4,则a为C元素,c为Si元素,d为Na或Mg或Al元素,据此解答该题.
解答 解:a、b、c、d都是短周期元素,原子半径d>c>a>b,其中a、b处在同一周期,a、c处在同一主族,可以判断a、b处于第二周期,c处于第三周期,a、c处在同一主族,二者质子数相差8,c原子核内质子数等于a、b原子核内质子数之和,故b的质子数为8,则b为O元素;c原子最外层上的电子数是d原子次外层电子数的一半,d不能处于第二周期,只能为第三周期元素,故c最外层电子数为4,则a为C元素,c为Si元素,d为Na或Mg或Al元素.
A.a为C元素,c为Si元素,最外层电子数为4,处于周期表第ⅣA族,故A错误;
B.b为O元素,若d为Na元素,二者可组成化合物Na2O2,且阴阳离子个数比为1:2,故B正确;
C.Si单质可在氧气中燃烧生成SiO2,故C正确;
D.用来制作光导纤维的SiO2,故D错误;
故选BC.
点评 本题考查结构性质与位置的关系等,题目难度中等,正确推断元素的种类为解答该题的关键,根据原子序数与半径关系确定大体位置,注意相关基础知识的积累.

练习册系列答案
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案
相关题目
20.下列叙述中指定粒子数目一定大于NA的是( )
| A. | 1mol苯分子中含有双键数 | |
| B. | 1mol CaC2固体中含阴离子总数 | |
| C. | 1L 1mol/L CH3COOH溶液中所含分子总数 | |
| D. | 1mol Cl2参加化学反应获得的电子数 |
1.下列解释实验现象的反应方程式正确的是( )
| A. | 向硫酸铝溶液中滴加过量的氨水:Al3++4OH-═AlO2-+2H2O | |
| B. | 金属铜与浓硝酸反应:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O | |
| C. | 实验室制备氢氧化铁胶体:Fe3++3H2O═Fe(OH)3(胶体)+3H+ | |
| D. | 向苯酚钠溶液中通入少量的二氧化碳气体:2C6H5ONa+CO2+H2O═2C6H6O+Na2CO3 |
18. (1)一定条件下,向一带活塞的密闭容器中充入2mol SO2和1mol O2发生反应:2SO2(g)+O2(g)═2SO3(g),下列说法中,正确的是C.
(1)一定条件下,向一带活塞的密闭容器中充入2mol SO2和1mol O2发生反应:2SO2(g)+O2(g)═2SO3(g),下列说法中,正确的是C.
A.若υ正(O2)=2υ逆(SO3),说明该可逆反应已达到平衡状态
B.保持温度和容器体积不变,充入2mol N2,化学反应速率加快
C.平衡后移动活塞压缩气体,达到新平衡时SO2、O2的百分含量减小,SO3的百分含量增大
D.达平衡后,保持温度和容器体积不变,再充入2mol SO2,化学平衡向右移动,SO2的转化率增大.
(2)尾气SO2用NaOH溶液吸收后会生成Na2SO3.,实验测定常温下0.1mol/L Na2SO3溶液的pH为8,该溶液中由水电离出的氢氧根离子的浓度为10-6.
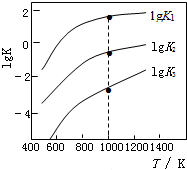
(3)煤炭中的硫主要以黄铁矿形式存在,用氢气脱除黄铁矿中硫的相关反应(见表),其相关反应的平衡常数的对数值与温度的关系如下.
①上述反应中,△H1>0(选填:“>”或“<”).其原因是温度升高,平衡常数增大.
②提高硫的脱除率可采取的措施有升高温度(举1例).
③1000K时,平衡常数的对数lgK1=lgK2-lgK3(用lgK2和lgK3来表示).
 (1)一定条件下,向一带活塞的密闭容器中充入2mol SO2和1mol O2发生反应:2SO2(g)+O2(g)═2SO3(g),下列说法中,正确的是C.
(1)一定条件下,向一带活塞的密闭容器中充入2mol SO2和1mol O2发生反应:2SO2(g)+O2(g)═2SO3(g),下列说法中,正确的是C.A.若υ正(O2)=2υ逆(SO3),说明该可逆反应已达到平衡状态
B.保持温度和容器体积不变,充入2mol N2,化学反应速率加快
C.平衡后移动活塞压缩气体,达到新平衡时SO2、O2的百分含量减小,SO3的百分含量增大
D.达平衡后,保持温度和容器体积不变,再充入2mol SO2,化学平衡向右移动,SO2的转化率增大.
(2)尾气SO2用NaOH溶液吸收后会生成Na2SO3.,实验测定常温下0.1mol/L Na2SO3溶液的pH为8,该溶液中由水电离出的氢氧根离子的浓度为10-6.
(3)煤炭中的硫主要以黄铁矿形式存在,用氢气脱除黄铁矿中硫的相关反应(见表),其相关反应的平衡常数的对数值与温度的关系如下.
| 相关反应 | 反应热 | 平衡常数K |
| FeS2(s)+H2(g)?FeS(s)+H2S(g) | △H1 | K1 |
| $\frac{1}{2}$FeS2(s)+H2(g)?$\frac{1}{2}$Fe(s)+H2S(g) | △H2 | K2 |
| FeS(s)+H2(g)?Fe(s)+H2S(g) | △H3 | K3 |
②提高硫的脱除率可采取的措施有升高温度(举1例).
③1000K时,平衡常数的对数lgK1=lgK2-lgK3(用lgK2和lgK3来表示).
15.常温下,某NH4Cl溶液的pH=4,下列说法中正确的是( )
①溶液中c(H+)>c(OH-);
②由水电离产生的c(H+)约为10-10mol/L;
③溶液中离子浓度关系为c(Cl-)>c(NH4+)>c(H+)>c(OH-);
④在纯水中加入该NH4Cl溶液,水的电离被抑制.
①溶液中c(H+)>c(OH-);
②由水电离产生的c(H+)约为10-10mol/L;
③溶液中离子浓度关系为c(Cl-)>c(NH4+)>c(H+)>c(OH-);
④在纯水中加入该NH4Cl溶液,水的电离被抑制.
| A. | ①② | B. | ①③ | C. | ①④ | D. | ①②③④ |
16.下列反应中,反应后固体物质质量不变的是( )
| A. | 氢气通过灼热的CuO粉末 | B. | 二氧化碳通过Na2O2粉末 | ||
| C. | 铝与Fe2O3发生铝热反应 | D. | 将锌粒投入Cu(NO3)2溶液 |
 .
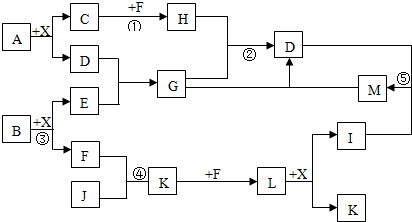
.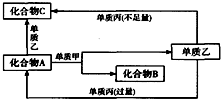 A、B、C都是由两种元素组成的无机物,它们和单质甲、乙、丙在如图所示的转化关系(转化过程都不需要使用催化剂).
A、B、C都是由两种元素组成的无机物,它们和单质甲、乙、丙在如图所示的转化关系(转化过程都不需要使用催化剂).