题目内容
高铁酸钾(K2FeO4)有强氧化性,是一种安全性很高的水处理剂。
(1)高铁酸钾中铁元素的化合价是 ,它可以将废水中的亚硝酸钾(KNO2)氧化,同时生成具有吸附性的Fe(OH)3,该反应的化学方程式为 。
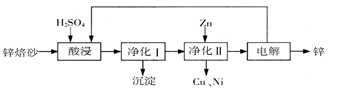
(2)某学习小组用废铁泥(主要成分为Fe3O3、FeO、CuO和少量Fe)制备高铁酸钾的流程如下:

①操作Ⅰ要在通风橱中进行,其原因是 。
②溶液A中含有的金属阳离子是 。
③25℃时,若将溶液B中的金属离子完全沉淀,应调节c(H+)小于 。(已知:i. Ksp[Fe(OH)3]=2.7×10-39、Ksp[Fe(OH)2] =4.0×10-17、Ksp[Cu(OH)2] =1.6×10-20;ii. 溶液中离子浓度小于10-5 mol·L-1时,可视为沉淀完全。)
④该小组经多次实验,得到如图结果,他们的实验目的是 。
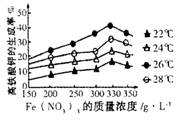
(3)高铁酸钾还可以用电解法制取,电解池以铁丝网为阳极,电解液使用氢氧化钾溶液,其阳极反应式为 。
(1)高铁酸钾中铁元素的化合价是 ,它可以将废水中的亚硝酸钾(KNO2)氧化,同时生成具有吸附性的Fe(OH)3,该反应的化学方程式为 。
(2)某学习小组用废铁泥(主要成分为Fe3O3、FeO、CuO和少量Fe)制备高铁酸钾的流程如下:

①操作Ⅰ要在通风橱中进行,其原因是 。
②溶液A中含有的金属阳离子是 。
③25℃时,若将溶液B中的金属离子完全沉淀,应调节c(H+)小于 。(已知:i. Ksp[Fe(OH)3]=2.7×10-39、Ksp[Fe(OH)2] =4.0×10-17、Ksp[Cu(OH)2] =1.6×10-20;ii. 溶液中离子浓度小于10-5 mol·L-1时,可视为沉淀完全。)
④该小组经多次实验,得到如图结果,他们的实验目的是 。

(3)高铁酸钾还可以用电解法制取,电解池以铁丝网为阳极,电解液使用氢氧化钾溶液,其阳极反应式为 。
(1)+6 (2分) 2 K2FeO4 + 3KNO2 +5H2O =" 2" Fe(OH)3+3KNO3 + 4KOH (3分)
(2) ①反应产生的氮氧化物有毒 (2分)
②Fe3+、Cu2+(2分)
③2.5×10-7 mol·L-1 (2分)
④探究高铁酸钾的生成率随温度、硝酸铁的质量浓度的变化关系(2分)
(3)Fe+8OH--6e-=FeO42-+4H2O (3分)
试题分析:(1)根据化合价代数和为零计算得出;(2)①硝酸被还原为NO、NO2等有毒气体污染空气故应在通风橱中进行实验;②硝酸过量,铁元素应生成Fe3+,铜为Cu2+;③操作Ⅱ使Fe3+沉淀,而Cu2+不沉淀留在溶液中,若使B溶液中铜离子沉淀完全,则有,Ksp[Cu(OH)2] = c2(OH-)×c(Cu2+)=1.6×10-20 c2(OH-)=1.6×10-20÷10-5
c(OH-)=4×10-8 mol·L-1
c(H+)=.5×10-7 mol·L-1
当氢离子浓度大于等于.5×10-7 mol·L-1时可以认为氢氧化铜沉淀完全;
④实验需要的是产物的生成率(纵坐标),另外还有两个变量分别是温度和反应物的浓度,显然是探究高铁酸钾的生成率随温度、硝酸铁的质量浓度的变化关系;
(3)活泼金属铁为阳极,铁失去电子生成FeO42-,介质为碱性,电极反应式为Fe+8OH--6e-=FeO42-+4H2O。

练习册系列答案
相关题目

 的溶液中肯定不存在Ag+
的溶液中肯定不存在Ag+ CuS(s)+Mn2+(aq),下列说法错误的是
CuS(s)+Mn2+(aq),下列说法错误的是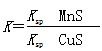

 。
。