题目内容
硫化钠主要用于皮革、毛纺、高档纸张、染料等行业.生产硫化钠大多采用无水芒硝(Na2SO4)-炭粉还原法,其流程示意图如下: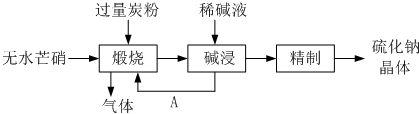
(1)上述流程中“碱浸”后,物质A必须经过
(2)上述流程中采用稀碱液比用热水更好,理由是
(3)取硫化钠晶体(含少量NaOH)加入到硫酸铜溶液中,充分搅拌.若反应后测得溶液的pH=4,则此时溶液中c(S2-)=
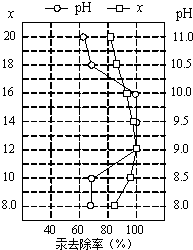 (4)①皮革工业废水中的汞常用硫化钠除去,汞的去除率与溶液的pH和x(x代表硫化钠的实际用量与理论用量的比值)有关(如图所示).为使除汞效果最佳,应控制的条件是
(4)①皮革工业废水中的汞常用硫化钠除去,汞的去除率与溶液的pH和x(x代表硫化钠的实际用量与理论用量的比值)有关(如图所示).为使除汞效果最佳,应控制的条件是②某毛纺厂废水中含0.001mol?L-1的硫化钠,与纸张漂白后的废水(含0.002mol?L-1 NaClO)按1:2的体积比混合,能同时较好处理两种废水,处理后的废水中所含的主要阴离子有
(2)依据硫化钠溶液中硫离子水解显碱性的水解平衡影响因素分析判断;
(3)常温时CuS、Cu(OH)2的Ksp,依据溶度积常数计算得到,依据溶液PH计算溶液中铜离子浓度,依据CuS的Ksp计算得到硫离子的浓度;
(4)①依据图象中曲线分析,汞去除率最佳PH和x的取值;
②依据硫化钠和次氯酸钠在溶液中发生的氧化还原反应电子守恒计算分析判断.
| 3 |
| 4 |
| ||
| 3 |
| 4 |
| ||
故答案为:过滤;3Na2SO4+8C
| ||
(2)上述流程中采用稀碱液比用热水更好,硫化钠溶液中硫离子水解显碱性,水解过程是吸热反应,加热促进水解进行,稀碱溶液能起到抑制水解的作用,
故答案为:热水会促进Na2S水解,而稀碱液能抑制Na2S水解;
(3)取硫化钠晶体(含少量NaOH)加入到硫酸铜溶液中,充分搅拌.若反应后测得溶液的pH=4,常温时CuS、Cu(OH)2的Ksp分别为8.8×10-36、2.2×10-20,
Ksp=c(Cu2+)×c2(OH-)=2.2×10-20,pH=4,c(OH-)=10-10mol/L,c(Cu2+)=2.2mol/L,硫化铜中的Ksp=c(Cu2+)c(S2-)=8.8×10-36、计算得到c(S2-)=4×10-36mol/L;
故答案为:4×10-36;
(4)①依据图象中曲线分析,汞去除率最佳PH和x的取值是x=12 pH介于9~10之间时汞的去除率最大,接近100%;
故答案为:x=12 pH介于9~10之间
②某毛纺厂废水中含0.001mol?L-1的硫化钠,与纸张漂白后的废水(含0.002mol?L-1 NaClO)按1:2的体积比混合,能同时较好处理两种废水,次氯酸钠和硫化钠发生氧化还原反应,n(Na2S):n(NaClO)=0.001mol/L×1:0.002mol?L-1×2=1:4,依据电子守恒分析可知,Na2S+4NaClO=Na2SO4+4NaCl,处理后的废水中所含的主要阴离子有
SO42-、Cl-;
故答案为:SO42-、Cl-.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案含有硫的化合物在工业生产中应用广泛,回答下列问题:
(1)黄铜矿是工业炼铜的主要原料,其主要成分为CuFeS2。
①测得某黄铜矿(CuFeS2)中含硫20%(质量分数),求该矿石含铜的质量分数。
②现有一种天然黄铜矿(含少量脉石),为了测定该黄铜矿的纯度,某同学设计了如下实验:称取
研细的黄铜矿样品1.150g,在空气中进行煅烧,生成Cu、Fe3O4和SO2气体,用100 mL滴有淀粉的
蒸馏水全部吸收SO2,然后取10mL吸收液,用0.05mol/L标准碘溶液进行滴定,用去标准碘溶液的体
积为20.00mL。求该黄铜矿的纯度。
(2)将FeS和Fe2O3的混和物56.6 g,用足量稀H2SO4溶解后可得3.2 g硫,原混和物中FeS的质量。
(3)一定温度下,硫酸铜受热分解生成CuO、SO2、SO3和O2。已知:SO2、SO3都能被碱石灰和氢氧
化钠溶液吸收。利用下图装置加热无水硫酸铜粉末直至完全分解。若无水硫酸铜粉末质量为10.0 g,
完全分解后,各装置的质量变化关系如下表所示。
|
装置 |
A(试管+粉末) |
B |
C |
|
反应前 |
42.0 g |
75.0 g |
140.0 g |
|
反应后 |
37.0 g |
79.0 g |
140.5 g |

请通过计算,推断出该实验条件下硫酸铜分解的化学方程式。
(4)硫化钠是用于皮革的重要化学试剂,可用无水Na2SO4与炭粉在高温下反应制得,化学方程式如下:
①Na2SO4
+ 4C Na2S + 4CO↑ ②Na2SO4
+ 4CO
Na2S + 4CO↑ ②Na2SO4
+ 4CO Na2S + 4CO2
Na2S + 4CO2
a.若在反应过程中,产生CO和CO2混合气体为2mol,求生成Na2S的物质的量。
b.硫化钠晶体放置在空气中,会缓慢氧化成Na2SO3,甚至是Na2SO4,现将43.72g部分变质的硫化钠样品溶于水中,加入足量盐酸后,过滤得4.8g沉淀和1.12L H2S 气体(标准状况,假设溶液中气体全部逸出),在滤液中加入足量的BaCl2后过滤得2.33g沉淀,分析该硫化钠样品的成分及其物质的量。
 含有硫的化合物在工业生产中应用广泛,回答下列问题:
含有硫的化合物在工业生产中应用广泛,回答下列问题:
(1)黄铜矿是工业炼铜的主要原料,其主要成分为CuFeS2.
①测得某黄铜矿(CuFeS2)中含硫20%(质量分数),求该矿石含铜的质量分数.
②现有一种天然黄铜矿(含少量脉石),为了测定该黄铜矿的纯度,某同学设计了如下实验:称取研细的黄铜矿样品1.150g,在空气中进行煅烧,生成Cu、Fe3O4和SO2气体,用100mL滴有淀粉的蒸馏水全部吸收SO2,然后取10mL吸收液,用0.05mol/L标准碘溶液进行滴定,用去标准碘溶液的体积为20.00mL.求该黄铜矿的纯度.
(2)将FeS和Fe2O3的混和物56.6g,用足量稀H2SO4溶解后可得3.2g硫,求原混和物中FeS的质量.
(3)一定温度下,硫酸铜受热分解生成CuO、SO2、SO3和O2.已知:SO2、SO3都能被碱石灰和氢氧化钠溶液吸收.利用下图装置加热无水硫酸铜粉末直至完全分解.若无水硫酸铜粉末质量为10.0g,完全分解后,各装置的质量变化关系如下表所示.
| 装置 | A (试管+粉末) | B | C |
| 反应前 | 42.0g | 75.0g | 140.0g |
| 反应后 | 37.0g | 79.0g | 140.5g |
(4)硫化钠是用于皮革的重要化学试剂,可用无水Na2SO4与炭粉在高温下反应制得,化学方程式如下:
①Na2SO4+4C
 Na2S+4CO ②Na2SO4+4CO
Na2S+4CO ②Na2SO4+4CO Na2S+4CO2
Na2S+4CO2①若在反应过程中,产生CO和CO2混合气体为2mol,求生成Na2S的物质的量.
②硫化钠晶体放置在空气中,会缓慢氧化成Na2SO3,甚至是Na2SO4,现将43.72g部分变质的硫化钠样品溶于水中,加入足量盐酸后,过滤得4.8g沉淀和1.12L H2S 气体(标准状况,假设溶液中气体全部逸出),在滤液中加入足量的BaCl2后过滤得2.33g沉淀,分析该硫化钠样品的成分及其物质的量.
(1)黄铜矿是工业炼铜的主要原料,其主要成分为CuFeS2.
①测得某黄铜矿(CuFeS2)中含硫20%(质量分数),求该矿石含铜的质量分数.
②现有一种天然黄铜矿(含少量脉石),为了测定该黄铜矿的纯度,某同学设计了如下实验:称取研细的黄铜矿样品1.150g,在空气中进行煅烧,生成Cu、Fe3O4和SO2气体,用100mL滴有淀粉的蒸馏水全部吸收SO2,然后取10mL吸收液,用0.05mol/L标准碘溶液进行滴定,用去标准碘溶液的体积为20.00mL.求该黄铜矿的纯度.
(2)将FeS和Fe2O3的混和物56.6g,用足量稀H2SO4溶解后可得3.2g硫,求原混和物中FeS的质量.
(3)一定温度下,硫酸铜受热分解生成CuO、SO2、SO3和O2.已知:SO2、SO3都能被碱石灰和氢氧化钠溶液吸收.利用下图装置加热无水硫酸铜粉末直至完全分解.若无水硫酸铜粉末质量为10.0g,完全分解后,各装置的质量变化关系如下表所示.
| 装置 | A (试管+粉末) | B | C |
| 反应前 | 42.0g | 75.0g | 140.0g |
| 反应后 | 37.0g | 79.0g | 140.5g |
(4)硫化钠是用于皮革的重要化学试剂,可用无水Na2SO4与炭粉在高温下反应制得,化学方程式如下:
①Na2SO4+4C
 Na2S+4CO ②Na2SO4+4CO
Na2S+4CO ②Na2SO4+4CO Na2S+4CO2
Na2S+4CO2①若在反应过程中,产生CO和CO2混合气体为2mol,求生成Na2S的物质的量.
②硫化钠晶体放置在空气中,会缓慢氧化成Na2SO3,甚至是Na2SO4,现将43.72g部分变质的硫化钠样品溶于水中,加入足量盐酸后,过滤得4.8g沉淀和1.12L H2S 气体(标准状况,假设溶液中气体全部逸出),在滤液中加入足量的BaCl2后过滤得2.33g沉淀,分析该硫化钠样品的成分及其物质的量.

 (2013?闸北区二模)含有硫的化合物在工业生产中应用广泛,回答下列问题:
(2013?闸北区二模)含有硫的化合物在工业生产中应用广泛,回答下列问题: