题目内容
9.(1)将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流计.锌片作负极,发生的电极反应式为Zn-2e-═Zn2+
银片上正极,发生的电极反应类型为2H++2e-═H2↑
(2)若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为53.5g,试计算:
①产生氢气的体积(标准状况)2.24L;②消耗的锌的质量6.5g.
分析 (1)将锌片和银片浸入稀硫酸中组成原电池,锌做负极,失电子发生氧化反应,银片做正极,溶液中氢离子在银电极得到电子发生还原反应;
(2)依据该电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47g,分析判断电极质量减小为反应的锌的质量为13g,依据电极反应和电子守恒计算生成的气体物质的量得到气体体积,依据电子转移物质的量换算导线的电子.
解答 解:(1)将锌片和银片浸入稀硫酸中组成原电池,锌做负极,失电子发生氧化反应,电极反应为:Zn-2e-═Zn2+,银片做正极,溶液中氢离子在银电极得到电子发生还原反应,电极反应为:2H++2e-═H2↑,
故答案为:负;Zn-2e-═Zn2+;正;2H++2e-═H2↑;
(2)若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为53.5g,分析可知电极质量减小的是负极反应的锌的质量,物质的量=$\frac{60g-53.5g}{65g/mol}$=0.1mol;
①锌做负极,失电子发生氧化反应,电极反应为:Zn-2e-═Zn2+,银片做正极,溶液中氢离子在银电极得到电子发生还原反应,电极反应为:2H++2e-═H2↑,依据电子守恒可知,转移电子物质的量为0.2mol,生成氢气物质的量为0.1mol,标准状况下体积=0.1mol×22.4L/mol=2.24L,
故答案为:2.24;
②依据计算可知转移电子物质的量为0.2mol,锌做负极,失电子发生氧化反应,电极反应为:Zn-2e-═Zn2+,消耗Zn的质量为6.5g,故答案为:6.5.
点评 本题考查了原电池原理的分析判断,电极反应,电极名称,电子守恒的计算应用,掌握基础是解题关键,题目较简单.

练习册系列答案
相关题目
17.有关原子最外层电子排布为(n+1)sn(n+1)pn+1的元素及其化合物,下列叙述中不正确的是( )
| A. | 氢化物不稳定 | |
| B. | 最高价氧化物对应的水化物是一种强酸 | |
| C. | 其单质既有氧化性又有还原性 | |
| D. | 是植物生长所需要的一种营养元素 |
4.下列有机物命名正确的是( )
| A. | 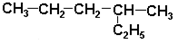 2-乙基戊烷 2-乙基戊烷 | B. |  2-甲基-2-氯丙烷 2-甲基-2-氯丙烷 | ||
| C. | 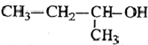 2-甲基-1-丙醇 2-甲基-1-丙醇 | D. |  2-甲基-3-丁炔 2-甲基-3-丁炔 |
18.20g AO32-中核外电子数比质子数多0.5NA(NA代表阿伏加德罗常数)个,则元素A的相对原子质量为( )
| A. | 12 | B. | 32 | C. | 60 | D. | 80 |
19.福岛核电站泄漏的放射性物质中含有${\;}_{53}^{131}$I,下列有关${\;}_{53}^{131}$I的说法正确的是( )
| A. | 由此可确定碘元素的相对原子质量为131 | |
| B. | ${\;}_{53}^{131}$I是碘元素的一种核素 | |
| C. | ${\;}_{53}^{131}$I核素中含中子数为53 | |
| D. | ${\;}_{53}^{131}$I2的摩尔质量为262g |

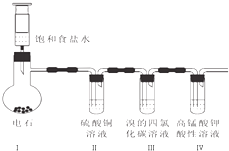 实验室制乙炔并检验其性质的装置如图.
实验室制乙炔并检验其性质的装置如图.