题目内容
8.银耳本身为淡黄色,福建省出产一种雪耳,颜色洁白如雪.其制作过程如下:将银耳堆放在密封状况良好的塑料棚内,在棚的一端置一口锅,锅内放硫磺,加热使硫磺熔化并燃烧,两天左右,雪耳就制成了.这种雪耳是对人体有害的.制作雪耳利用了( )| A. | 硫的还原性 | B. | 硫的氧化性 | ||
| C. | 二氧化硫的还原性 | D. | 二氧化硫的漂白性 |
分析 二氧化硫属于酸性氧化物,具有氧化性、还原性,能和有色物质反应生成无色物质而具有漂白性,据此分析解答.
解答 解:二氧化硫属于酸性氧化物;
能和硫化物溶液反应生成S单质沉淀而体现氧化性;
能被高锰酸钾溶液、溴水等氧化而体现还原性;
能和有色物质反应生成无色物质而具有漂白性,银耳被二氧化硫漂白是利用二氧化硫的漂白性,故选D.
点评 本题考查二氧化硫的性质,明确二氧化硫漂白原理是解本题关键,注意二氧化硫漂白性是暂时的,且不能漂白酸碱指示剂.

练习册系列答案
相关题目
16.比较Al和Mg这两种金属强弱性的方法是( )
| A. | 比较这两种元素的单质的硬度和熔点 | |
| B. | 在氯化铝和氯化镁的溶液中分别滴加过量的氢氧化钠溶液 | |
| C. | 将打磨过的镁带和铝片分别和热水作用,并滴入酚酞溶液 | |
| D. | 将空气中放置已久的这两种元素的单质分别和热水作用 |
16.今有两种正盐的稀溶液,分别是a mol/LNaX溶液和b mol/LNaY溶液,下列说法不正确的是( )
| A. | 若a=b,pH(NaX)>pH(NaY),则相同浓度时,酸性HX<HY | |
| B. | 若a=b,并测得c(X-)=c(Y-)+c(HY),则相同浓度时,酸性HX>HY | |
| C. | 若a>b,测得c(X-)=c(Y-),则可推出溶液中c(HX)>c(HY),且相同浓度时,酸性HX<HY | |
| D. | 若两溶液等体积混合,测得c(X-)+c(Y-)+c(HX)+c(HY)=0.1mol/L,则可推出a=b=0.1 mol/L |
13.下列有机物名称中,符合系统命名法的是( )
| A. | 1,2,3-丙三醇 | B. | 1-甲基-5-乙基苯 | ||
| C. | 3-甲基-2-乙基戊烷 | D. | 2-甲基-1,3-丁二烯 |
20.下列说法正确的是( )
| A. | 硫粉在过量的纯氧中燃烧可以生成SO3 | |
| B. | 可以用澄清石灰水鉴别SO2和CO2 | |
| C. | SO2能使酸性KMnO4水溶液褪色,是因为SO2有漂白性 | |
| D. | 铁粉与过量硫粉反应生成硫化亚铁 |
17.如图水槽中盛装的是海水,其中铁被腐蚀最慢的是( )
| A. | 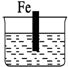 | B. | 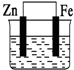 | C. |  | D. | 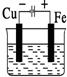 |
18.一定质量的铜分别与足量的浓硝酸和稀硝酸完全反应,在相同条件下用排水法收集产生的气体,下列叙述正确的是( )
| A. | 硝酸浓度越大,反应消耗的硝酸越少 | |
| B. | 硝酸浓度越大,产生的气体越少 | |
| C. | 硝酸浓度不同,生成Cu(NO3)2的物质的量不同 | |
| D. | 两者用排水法收集到气体体积相等 |

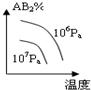

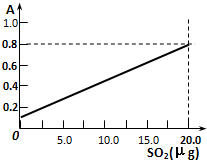 某省2005年工业(主要是热电厂)二氧化硫排放总量为1.24×106 t,全省酸雨污染比较严重.分析降雨成分发现,雨水中阴离子仍以硫酸根离子为主,约占阴离子总量的61.9%,阳离子以铵根离子为主,约占阳离子总量的84.1%.阴离子中SO42-和NO3-的质量比为4.13:1,NO3-的比例呈明显上升的趋势.回答下列问题:
某省2005年工业(主要是热电厂)二氧化硫排放总量为1.24×106 t,全省酸雨污染比较严重.分析降雨成分发现,雨水中阴离子仍以硫酸根离子为主,约占阴离子总量的61.9%,阳离子以铵根离子为主,约占阳离子总量的84.1%.阴离子中SO42-和NO3-的质量比为4.13:1,NO3-的比例呈明显上升的趋势.回答下列问题: