题目内容
已知2H2+O2
2H2O,关于该反应的下列说法错误的是( )
| ||
| A、该反应是一个放热反应 |
| B、参加反应的氢气和氧气的总能量高于反应生成的水的总能量 |
| C、水分解为氢气和氧气需要吸收能量 |
| D、断键所吸收的总能量高于成键所放出的能量 |
分析:A、氢气在氧气中燃烧是放热反应;
B、反应物总能量高于生成物,反应放热;
C、水分解需要吸收能量;
D、反应中断裂化学键吸收的能量低于形成化学键放出的能量,反应放热.
B、反应物总能量高于生成物,反应放热;
C、水分解需要吸收能量;
D、反应中断裂化学键吸收的能量低于形成化学键放出的能量,反应放热.
解答:解:A、氢气在氧气中点燃发生燃烧,是放热反应,故A正确;
B、反应是放热反应,依据反应前后能量守恒得到,反应物总能量高于生成物,故B正确;
C、氢气和氧气反应是放热反应,逆向反应是吸热反应,水分解需要吸收能量,故C正确;
D、反应是放热反应,所以反应中断裂化学键吸收的能量低于形成化学键放出的能量,故D错误;
故选D.
B、反应是放热反应,依据反应前后能量守恒得到,反应物总能量高于生成物,故B正确;
C、氢气和氧气反应是放热反应,逆向反应是吸热反应,水分解需要吸收能量,故C正确;
D、反应是放热反应,所以反应中断裂化学键吸收的能量低于形成化学键放出的能量,故D错误;
故选D.
点评:本题考查了化学反应能量变化分析,主要是能量守恒和反应实质的理解应用,题目较简单.

练习册系列答案
相关题目
 (2013?泰安三模)SO2、NO、NO2、CO都是污染大气的有害气体,对其进行回收利用是节能减排的重要课题.
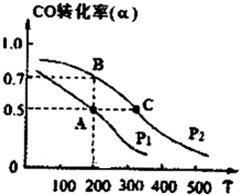
(2013?泰安三模)SO2、NO、NO2、CO都是污染大气的有害气体,对其进行回收利用是节能减排的重要课题. CH3OH(g);CO的转化率(α)与温度、压强的关系如图所示.
CH3OH(g);CO的转化率(α)与温度、压强的关系如图所示.
 (2013?淄博一模)请运用化学反应原理的相关知识研究元素及其化合物的性质.
(2013?淄博一模)请运用化学反应原理的相关知识研究元素及其化合物的性质.
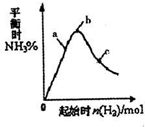 工业上利用N2和H2可以合成NH3,NH3又可以进一步制备联氨(N2H4)等.
工业上利用N2和H2可以合成NH3,NH3又可以进一步制备联氨(N2H4)等.