题目内容
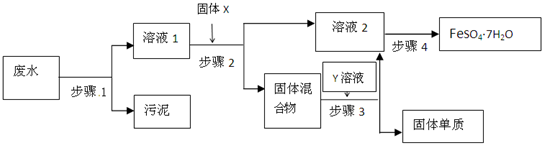
(12分)已知某工业废水中含有大量CuSO4,少量的Ag+、Hg2+以及部分污泥,通过下述过程可从该废水中回收硫酸铜晶体及其它物质。(汞在常温下是液态)
 (1)步骤1的主要操作是 ,需用到的玻璃仪器除烧杯外有 。
(1)步骤1的主要操作是 ,需用到的玻璃仪器除烧杯外有 。
(2)步骤2中需加入某种试剂后再将混合物分离,该试剂是(填化学式) ,固体残渣的成分是(填化学式) ;加入的试剂必须要过量,原因是:
(3)步骤3中涉及的操作是:蒸发浓缩、 、过滤、烘干。
(12分,每空2分)
(1)过滤(2分), 漏斗、玻璃棒(2分)
(2)Cu(2分), Ag、Cu(2分)
保证溶液中Ag+,Hg2+能反应完全 (2分)
(3)冷却结晶(2分)
解析

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目



 已知某工业废水中含有N
已知某工业废水中含有N