题目内容
(2009?湘潭一模)根据下列事实完成下列反应方程式:
(1)AsH3是一种很强的还原剂.室温下,它能在空气中自燃,其氧化产物为As2O3,写出反应的化学方程式:
(2)白磷在一定条件下可被HClO3的水溶液氧化,生成磷的最高价态化合物,而氯元素被还原为最低价态,写出反应化学方程式
(3)稀硫酸与铜不反应,但在稀硫酸中加H2O2后,则可使铜顺利溶解,写出该反应的离子方程式:
(4)在火箭推进器中装有强还原剂(N2H4)和强氧化剂H2O2.当它们混合时,即产生大量氮气和水蒸气,并放出大量热.已知0.4mol液态肼和足量液态H2O2反应,生成氮气和水蒸气,放出256.65KJ的热量.写出此反应的热化学方程式:
(1)AsH3是一种很强的还原剂.室温下,它能在空气中自燃,其氧化产物为As2O3,写出反应的化学方程式:
2AsH3+3O2=As2O3+3H2O
2AsH3+3O2=As2O3+3H2O
.(2)白磷在一定条件下可被HClO3的水溶液氧化,生成磷的最高价态化合物,而氯元素被还原为最低价态,写出反应化学方程式
3P4+10HClO3+18H2O=10HCl+12H3PO4
3P4+10HClO3+18H2O=10HCl+12H3PO4
.(3)稀硫酸与铜不反应,但在稀硫酸中加H2O2后,则可使铜顺利溶解,写出该反应的离子方程式:
H2O2+Cu+2H+=Cu2++2H2O
H2O2+Cu+2H+=Cu2++2H2O
.(4)在火箭推进器中装有强还原剂(N2H4)和强氧化剂H2O2.当它们混合时,即产生大量氮气和水蒸气,并放出大量热.已知0.4mol液态肼和足量液态H2O2反应,生成氮气和水蒸气,放出256.65KJ的热量.写出此反应的热化学方程式:
N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.625 kJ?mol-1
N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.625 kJ?mol-1
.分析:(1)AsH3与氧气反应生成As2O3和水;
(2)由题给信息可知白磷与HClO3的水溶液反应生成H3PO4和HCl;
(3)酸性条件下,过氧化氢和铜反应生成水和铜离子;
(4)计算1mol液态肼与足量液态双氧水反应时放出的热量,可写出反应的热化学方程式.
(2)由题给信息可知白磷与HClO3的水溶液反应生成H3PO4和HCl;
(3)酸性条件下,过氧化氢和铜反应生成水和铜离子;
(4)计算1mol液态肼与足量液态双氧水反应时放出的热量,可写出反应的热化学方程式.
解答:解:(1)AsH3与氧气反应生成As2O3和水,反应的方程式为2AsH3+3O2=As2O3+3H2O,故答案为:2AsH3+3O2=As2O3+3H2O;
(2)由题给信息可知白磷与HClO3的水溶液反应生成H3PO4和HCl,反应的方程式为3P4+10HClO3+18H2O=10HCl+12H3PO4,
故答案为:3P4+10HClO3+18H2O=10HCl+12H3PO4;
(3)酸性条件下Cu与过氧化氢发生氧化还原反应生成硫酸铜和水,反应的离子反应为H2O2+Cu+2H+=Cu2++2H2O,故答案为:H2O2+Cu+2H+=Cu2++2H2O;
(4)0.4mol液态肼和足量H2O2反应,生成氮气和水蒸气,放出256.65kJ的热量,1mol液态肼与足量液态双氧水反应时放出的热量641.625kJ,则热化学方程式为:N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.625 kJ?mol-1,
故答案为:N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.625 kJ?mol-1.
(2)由题给信息可知白磷与HClO3的水溶液反应生成H3PO4和HCl,反应的方程式为3P4+10HClO3+18H2O=10HCl+12H3PO4,
故答案为:3P4+10HClO3+18H2O=10HCl+12H3PO4;
(3)酸性条件下Cu与过氧化氢发生氧化还原反应生成硫酸铜和水,反应的离子反应为H2O2+Cu+2H+=Cu2++2H2O,故答案为:H2O2+Cu+2H+=Cu2++2H2O;
(4)0.4mol液态肼和足量H2O2反应,生成氮气和水蒸气,放出256.65kJ的热量,1mol液态肼与足量液态双氧水反应时放出的热量641.625kJ,则热化学方程式为:N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.625 kJ?mol-1,
故答案为:N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.625 kJ?mol-1.
点评:本题考查离子反应方程式的书写,明确发生的化学反应是解答本题的关键,注意氧化还原反应的发生,题目难度不大.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案
相关题目
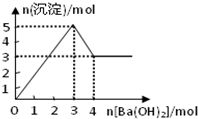 (2009?湘潭一模)如图表示在某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系.该溶液的成分可能是( )
(2009?湘潭一模)如图表示在某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系.该溶液的成分可能是( )
 (2009?湘潭一模)将2.5g碳酸钠、碳酸氢钠和氢氧化钠的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol?L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如图所示:
(2009?湘潭一模)将2.5g碳酸钠、碳酸氢钠和氢氧化钠的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol?L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如图所示: