题目内容
| A.1.3 g·L-1 | B.1.5 g·L-1 |
| C.1.7 g·L-1 | D.1.9 g·L-1 |
B
根据质量守恒定律,反应前后气体的总质量保持不变;反应前的质量为: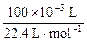 ×32 g·mol-1。终态时的密度为:0.143 g÷0.095 L="1.5" g·L-1。
×32 g·mol-1。终态时的密度为:0.143 g÷0.095 L="1.5" g·L-1。
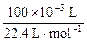 ×32 g·mol-1。终态时的密度为:0.143 g÷0.095 L="1.5" g·L-1。
×32 g·mol-1。终态时的密度为:0.143 g÷0.095 L="1.5" g·L-1。
练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案
相关题目
题目内容
| A.1.3 g·L-1 | B.1.5 g·L-1 |
| C.1.7 g·L-1 | D.1.9 g·L-1 |
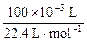 ×32 g·mol-1。终态时的密度为:0.143 g÷0.095 L="1.5" g·L-1。
×32 g·mol-1。终态时的密度为:0.143 g÷0.095 L="1.5" g·L-1。
 活力课时同步练习册系列答案
活力课时同步练习册系列答案