题目内容
下列实验事实能用平衡移动原理解释的是( )
A、
| ||||||||
B、
| ||||||||
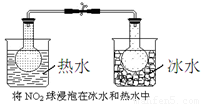
C、 将NO2球浸泡在冰水和热水中 | ||||||||
D、 |
分析:平衡移动原理主要内容为:在一个已经达到平衡的反应中,如果改变影响平衡的条件之一(如温度、压强,以及参加反应的化学物质的浓度),平衡将向着能够减弱这种改变的方向移动,能用平衡移动原理解释,首先必须存在可逆过程,以此解答该题.
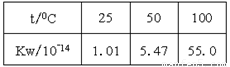
解答:解:A.水的电离为吸热过程,升高温度,平衡向正向移动,水的离子积常数增大,可用平衡移动原理解释,故A正确;
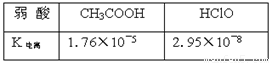
B.乙酸和次氯酸的电离常数不同,为物质的本身性质,与平衡移动原理无关,故B错误;
C.2NO2(g)?N2O4(g)正反应为放热反应,升高温度平衡向逆反应移动,颜色加深,可用平衡移动原理解释,故C正确;
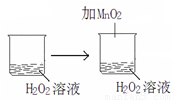
D.加入催化剂,平衡不发生移动,不能用平衡移动原理解释,故D错误.
故选AC.
B.乙酸和次氯酸的电离常数不同,为物质的本身性质,与平衡移动原理无关,故B错误;
C.2NO2(g)?N2O4(g)正反应为放热反应,升高温度平衡向逆反应移动,颜色加深,可用平衡移动原理解释,故C正确;
D.加入催化剂,平衡不发生移动,不能用平衡移动原理解释,故D错误.
故选AC.
点评:本题考查了勒夏特列原理的使用条件,难度不大,注意使用勒夏特列原理的前提必须是可逆反应,题中易错点为B和D,注意反应方程式的特征以及工业生成的实际等问题.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
下列实验事实不能用平衡移动原理解释的是( )
A、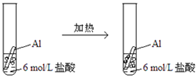 | ||||||
B、
| ||||||
C、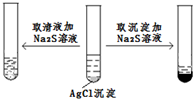 | ||||||
D、
|
下列实验事实不能用平衡移动原理解释的是( )
| A、配制FeSO4溶液时,加入一些铁粉 | ||||||||
B、
| ||||||||
C、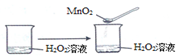 | ||||||||
D、
|