题目内容
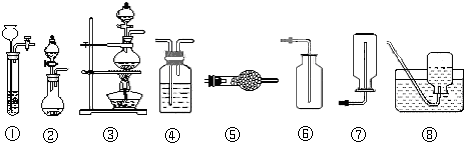
下列是实验室常见的气体制取、干燥和收集装置.若用过氧化氢和催化剂二氧化锰制取干燥的氧气,则合理的装置组合为( )

分析:用过氧化氢和催化剂二氧化锰制取干燥的氧气反应方程式为2H2O2
2H2O+O2↑,需要选用固液不加热装置,干燥氧气可用浓硫酸或碱石灰,要制取干燥的O2只能用排空气法,据此即可解答.
| ||
解答:解:用H2O2制O2的反应原理为2H2O2
2H2O+O2↑,过氧化氢为液态,二氧化锰为粉末状,由反应物的状态和反应条件可选②作为制取装置,干燥O2可选用④用浓硫酸的吸水性进行干燥,或用⑤装置用碱石灰进行干燥,要制取干燥的O2只能用⑥装置利用氧气密度比空气大采用向上排空气法收集,故合理的装置组合为②⑤⑥,
故选C.
| ||
故选C.
点评:本题考查化学实验操作实验室制氧气,注意理解装置各部分的作用是解题的关键,题目难度不大.

练习册系列答案
相关题目
(12分)在浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙(粒子直径在1~10nm之间).下图所示A~E为实验室常见的仪器装置(部分固定夹持装置略去),请根据要求回答问题.
(1)实验室制取、收集干燥的NH3,需选用上述仪器装置的接口连接顺序是(选填字母):a接 , 接 , 接h;
(2)向浓CaCl2溶液中通入NH3和CO2气体制纳米级碳酸钙时,应先通入的气体是 ,试写出制纳米级碳酸钙的离子方程式 ;
(3)在浓CaCl2溶液和NH3用量正确的情况下,CO2不足或过量都会导致纳米级碳酸钙产量下降,若CO2过量溶液中大量存在的离子有(不考虑弱电解质的电离和盐类水解产生的少量离子)_____________________________,
(4)取反应后去除CaCO3的溶液分别做以下实验,下列实验判断合理的是:_________.
| A.滴加少量Na2CO3溶液,若有沉淀说明CO2一定不足. |
| B.滴加少量盐酸,若有气泡,CO2一定过量. |
| C.测量溶液pH,若小于7,CO2一定过量 |
| D.滴加少量BaCl2溶液,若无沉淀,CO2一定没有过量. |



