题目内容
NA表示阿伏加德罗常数的值,下列有关说法正确的是
| A.标准状况下,22.4 LCH4和CH3CH2OH的混合物所含分子数为NA |
| B.常温常压下,16g14CH4所含中子数目为8 NA |
| C.含0.2 NA个阴离子的Na2O2和水完全反应转移0.2 mol电子 |
| D.0.1 L 3 mol·L-1的NH4NO3溶液中含有的NH4+数目为0.3 NA |
C
试题分析:A、标准状况下,CH3CH2OH为非气体,22.4 LCH4和CH3CH2OH的混合物所含分子数大于NA,错误;B、常温常压下,14CH4的相对分子质量为18,16g14CH4的物质的量为8/9mol,所含中子数目为64/9NA,错误;C、含0.2 NA个阴离子的Na2O2的物质的量为0.2mol,和水完全反应转移0.2 mol电子,正确;D、NH4NO3为强酸弱碱盐,NH4+水解,0.1 L 3 mol·L-1的NH4NO3溶液中含有的NH4+数目小于0.3 NA,错误。

练习册系列答案
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案
相关题目


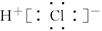
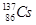
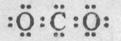
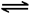 CO2(g)+H2(g) △H=-41kJ/mol,某温度下,向容积为2L的密闭容器中充入2.0molCO(g)和2.0molH2O(g),在tmin时达到平衡,测得放出了32.8kJ热量,则tmin内用H2表示的平均反应速率为 ,由此可知在该温度下反应CO2(g)+H2(g)
CO2(g)+H2(g) △H=-41kJ/mol,某温度下,向容积为2L的密闭容器中充入2.0molCO(g)和2.0molH2O(g),在tmin时达到平衡,测得放出了32.8kJ热量,则tmin内用H2表示的平均反应速率为 ,由此可知在该温度下反应CO2(g)+H2(g)