题目内容
下列有关实验装置进行的相应实验,能达到实验目的的是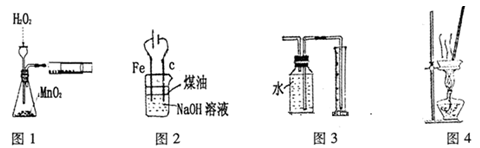
| A.图l装置可用于定量测定H2O2的分解速率 |
| B.图2装置制备Fe(OH)2并能较长时间观察其颜色 |
| C.图3装置测量Cu与浓硝酸反应产生气体的体积 |
| D.图4装置可用于蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
B
解析试题分析:A、图l装置可用于定量测定H2O2的分解速率,应用分液漏斗滴加双氧水,缺少秒表,错误;B、图2装置制备Fe(OH)2,阳极铁提供亚铁离子,氢氧化钠溶液提供氢氧根,煤油隔绝空气,能较长时间观察其颜色,正确;C、Cu与浓硝酸反应产生的二氧化氮气体易溶于水,不能用排水法量其体积,错误;D、NH4Cl水解生成一水合氨和盐酸,升高温度促进其水解,氨水和盐酸易挥发,蒸干NH4Cl饱和溶液得不到NH4Cl晶体,错误。
考点:考查实验方案的设计与评价。

 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案下列说法中正确的是( )
| A.常温下,浓硫酸、浓硝酸均能将金属铜氧化,且均能使铁钝化 |
| B.乙烯常用作植物催熟剂,乙酸常用作调味剂,乙醇常用于杀菌消毒 |
| C.玛瑙、水晶、钻石的主要成分均为SiO2 |
| D.用CCI4萃取碘水中的I2时,紫色溶液从分液漏斗的上口倒出 |
用18.4 mol·L-1的浓硫酸配制100 mL浓度为1 mol·L-1的稀硫酸,其操作可分为以下各步:
| A.用量筒量取5.4 mL浓硫酸,缓慢倒入装有约50 mL蒸馏水的烧杯里,并用玻璃棒搅拌 |
| B.用约30 mL蒸馏水,分成三次洗涤烧杯和玻璃棒,将洗涤液都倒入容量瓶中 |
| C.将稀释后的硫酸小心地倒入容量瓶中 |
| D.检查100 mL容量瓶口是否有漏液现象 |
F.盖紧瓶塞,反复颠倒振荡,摇匀溶液
G.用胶头滴管向容量瓶里逐滴加入蒸馏水,至液面最低点与刻度线相切
(1)正确的操作顺序应该是______________________________________________。
(2)进行A步操作的时候,应该选用的是________(填序号)。
①10 mL量筒;②50 mL量筒;③500 mL量筒;④1000 mL量筒
如果对装有浓硫酸的量筒读数如图所示,配制的稀硫酸的浓度将________(填“偏高”、“偏低”或“无影响”)。

(3)进行A步操作后,必须________,才能进行C步操作。
.(16分)化学实验是科学探究的基础。请回答有关实验问题:
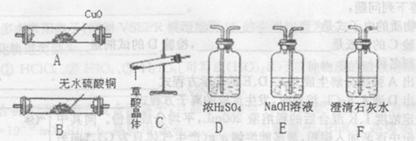
(1)下面的四个实验装置有三个都存在明显缺陷,其中完全正确的是 :
(2)要检验上面B装置氨气已集满的操作是 则试管已集满。
(3)ClO2是一种安全、高效、广谱、强力杀菌剂,其性质如右表:
①由下表可以看出:保存液态ClO2的条件是密封、 ;ClO2与碱反应的离子方程式 ;观察下“图A”,要从NaClO2溶液制得不含结晶水的晶体,操作是蒸发结晶,控制条件是 ;应控制析出晶体的温度范围是 。
| 色态 | 溶于碱 | 超过1Kpa、受热或遇光 | |
| 常温气体 | -59-11℃ 红黄色液体 | 生成亚氯酸盐和氯酸盐 | 爆炸 |
②工业用潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得。某学生拟用下图B所示装置模拟工业制法制取并收集液态ClO2,请模仿下图B的装置图和图例,在答题卡的相应图中补充完善装置图,并作必要的标注。

(4分)下列有关实验操作或判断不正确的是 _____________(填序号,多选扣分)。
| A.配制一定物质的量浓度溶液,定容时俯视刻度线会导致所配溶液浓度偏大 |
| B.少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗 |
| C.配制稀硫酸时,可先在烧杯中加入一定体积的蒸馏水,再边缓慢加入浓硫酸边搅拌 |
| D.100 mL容量瓶可用于配制95 mL 0.1 mol/L NaCl溶液 |
F.观察钾元素焰色反应的操作是:先将铂丝放在稀盐酸中洗涤,然后蘸取固体氯化钾,置于酒精灯的火焰上进行灼烧,透过蓝色钴玻璃进行观察。
G.苯、CCl4、酒精可用来萃取溴水中的溴。
(15分)S2Cl2常用于橡胶硫化、有机物氯化的试剂,实验室可利用如下装置来制备S2Cl2。(部分夹持仪器已略去)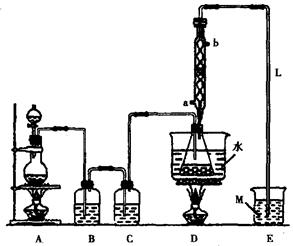
已知:①制备的反应方程式为: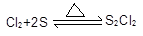
②反应涉及的几种物质性质如下:
| 性质 物质 | 熔点 | 沸点 | 着火点 | 其他性质 |
| 单斜硫 | 119.2℃ | 446.6℃ | 363℃ | / |
| 斜方硫 | 112.8℃ | 446.6℃ | 363℃ | / |
| S2Cl2 | -77℃ | 137℃ | / | 遇水强烈分解生成S、SO2和HCl |
(1)A部分仪器装配时,放好铁架台之后,应先固定 (填仪器名称)。整套装置装配完毕后,应先进行 ,再添加试剂,冷凝水进水口是 (填“a”或“b”)。实验完毕,A中不再产生氯气时,可拆除装置,拆除时,最先进行的操作应是 。
(2)S2Cl2分子中各原子均达到8电子稳定结构,写出其电子式 ;用化学方程式表示撤去C装置的后果 ;用直接加热代替水浴加热的后果是 。
(3)单斜硫、斜方硫互称为 ,从熔点、沸点、着火点等信息得到的启示是 。
(4)M溶液可以选择下列试剂中的 (填序号)
①碳酸钠溶液 ②氯化铁溶液 ③亚硫酸钠溶液 ④高锰酸钾溶液
PCl3可用于半导体生产的外延、扩散工序。有关物质的部分性质如下:
| | 熔点/℃ | 沸点/℃ | 密度/g·mL-1 | 其他 |
| 黄磷 | 44.1 | 280.5 | 1.82 | 2P(过量)+3Cl2 2PCl3;2P+5Cl2(过量) 2PCl3;2P+5Cl2(过量) 2PCl5 2PCl5 |
| PCl3 | -112 | 75.5 | 1.574 | 遇水生成H3PO3和HCl,遇O2生成POCl3 |
| POCl3 | 2 | 105.3 | 1.675 | 遇水生成H3PO4和HCl,能溶于PCl3 |
如图是实验室制备PCl3的装置(部分仪器已省略)。
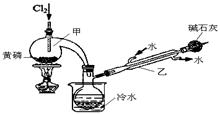
(1)向甲中通入干燥的Cl2之前,需先通入一段时间CO2,目的是 。
(2)实验过程中,应控制 ,以减少PCl5的生成。
(3)粗产品品中常含有POCl3、PCl5等。加入黄磷加热除去PCl5后,通过 (填实验操作名称),即可得到PCl3的纯品。
(4)已知:a.H3PO3+H2O+I2
 H3PO4+2HI;b.(NH4)3BO3溶液可与HI和H3PO4反应生成H3BO3(弱酸);c.Na2S2O3溶液可定量测定碘:I2+2Na2S2O3→Na2S4O6+2NaI
H3PO4+2HI;b.(NH4)3BO3溶液可与HI和H3PO4反应生成H3BO3(弱酸);c.Na2S2O3溶液可定量测定碘:I2+2Na2S2O3→Na2S4O6+2NaI①测定产品中PCl3质量分数的实验如下,请补充相应的实验步骤:
步骤1:迅速移取m g产品,水解完全后在500mL容量瓶中定容。
步骤2:从容量瓶中移取25.00mL溶液置于锥形瓶中。
步骤3:准确加入c1 mol/L碘溶液V1 mL(过量),再 。
步骤4:用标准Na2S2O3溶液回滴过量的碘,将近终点时加入3 mL淀粉溶液,继续滴至终点(蓝色溶液褪色);滴至终点时消耗c2 mol/L Na2S2O3溶液V2 mL。
②根据上述数据,该产品中PCl3的质量分数为 (用含字母的代数式表示)。
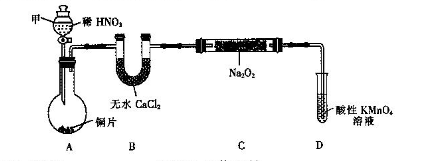
 ,发生反应的离子方程式为_____________。
,发生反应的离子方程式为_____________。