题目内容
1. CuCl是应用广泛的有机合成催化剂,可采取不同方法制取.
CuCl是应用广泛的有机合成催化剂,可采取不同方法制取.方法一 铜粉还原CuSO4溶液
CuSO4溶液$→_{加热①}^{NaCl、过量Cu粉、浓盐酸}$ $\stackrel{过滤}{→}$滤液 $→_{②}^{水}$ $\stackrel{过滤}{→}$滤渣$→_{92%乙醇}^{洗涤}$$\stackrel{真空干燥}{→}$CuCl
已知:CuCl难溶于水和乙醇,在水溶液中存在平衡:CuCl(白色)+2Cl-?[CuCl3]2-(无色溶液).
(1)将废铜板浸入热的H2SO4溶液中,并通入空气,可以生成CuSO4.该反应的离子方程式为2Cu+O2+4H+$\frac{\underline{\;\;△\;\;}}{\;}$2Cu2++2H2O.
(2)①中“加热”的目的是加快反应的速率,当观察到溶液由蓝色变为无色现象,即表明反应已经完全.
(3)②中加入大量水的作用是稀释促进平衡CuCl(白色)+2Cl-
 [CuCl3]2-(无色溶液)逆向移动,生成CuCl.
[CuCl3]2-(无色溶液)逆向移动,生成CuCl.(4)潮湿的CuCl在空气中易发生水解和氧化.上述流程中,为防止水解和氧化所添加的试剂或采取的操作是浓盐酸、95%乙醇、真空干燥.
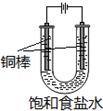
方法二 铜电极电解饱和食盐水(实验装置如图)
(5)阳极的电极反应式为Cu-e-+Cl-=CuCl.
(6)实验开始时,阳极附近没有产生CuOH沉淀的原因是阳极区Cl-浓度远远高于OH-的浓度.(已知:Ksp(CuCl)=1.2×10-6,Ksp(CuOH)=1.2×10-14)
分析 方法一:CuSO4溶液与NaCl、Cu粉、盐酸在加热条件反应得到[CuCl3]2-,过滤分离出未反应的Cu,滤液中含有CuCl3]2-,在水溶液中存在平衡:CuCl(白色)+2Cl-?[CuCl3]2-(无色溶液),加入水进行稀释,有利于CuCl沉淀的生成,再经过过滤分离,洗涤干燥得到CuCl.
(1)由题目信息可知,Cu、氧气与硫酸反应生成硫酸铜与水;
(2)加热可以加快反应速率,由于硫酸铜溶液为蓝色,而[CuCl3]2-为无色溶液,根据溶液颜色变化判断反应已经完全;
(3)加入水进行稀释,有利于CuCl沉淀的生成;
(4)潮湿的CuCl在空气中易发生水解和氧化,开始加入的浓盐酸及用酒精洗涤均可以抑制水解,在真空中干燥,不能与空气接触;
方法二:(5)利用电解原理制备CuCl,阳极发生氧化反应,Cu失去电子,与氯离子作用生成CuCl;
(6)由于Ksp(CuCl)远远大于Ksp(CuOH),开始没有CuOH生成,而是生成CuCl,说明氯离子浓度远远大于氢氧根离子浓度.
解答 解:方法一:CuSO4溶液与NaCl、Cu粉、盐酸在加热条件反应得到[CuCl3]2-,过滤分离出未反应的Cu,滤液中含有CuCl3]2-,在水溶液中存在平衡:CuCl(白色)+2Cl-?[CuCl3]2-(无色溶液),加入水进行稀释,有利于CuCl沉淀的生成,再经过过滤分离,洗涤干燥得到CuCl.
(1)由题目信息可知,Cu、氧气与硫酸反应生成硫酸铜与水,反应离子方程式为:2Cu+O2+4H+$\frac{\underline{\;\;△\;\;}}{\;}$2Cu2++2H2O,
故答案为:2Cu+O2+4H+$\frac{\underline{\;\;△\;\;}}{\;}$2Cu2++2H2O;
(2)升高温度,反应速率加快,①中“加热”的目的是:加快反应的速率,由于硫酸铜溶液为蓝色,而[CuCl3]2-为无色溶液,当观察到溶液由蓝色变为无色现象,即表明反应已经完全,
故答案为:加快反应的速率;溶液由蓝色变为无色;
(3)加入水进行稀释,促进平衡:CuCl(白色)+2Cl- [CuCl3]2-(无色溶液)逆向移动,生成CuCl,
[CuCl3]2-(无色溶液)逆向移动,生成CuCl,
故答案为:稀释促进平衡CuCl(白色)+2Cl- [CuCl3]2-(无色溶液)逆向移动,生成CuCl;
[CuCl3]2-(无色溶液)逆向移动,生成CuCl;
(4)潮湿的CuCl在空气中易发生水解和氧化,开始加入的浓盐酸及用酒精洗涤均可以抑制水解,在真空中干燥,不能与空气接触,防止氧化,
故答案为:浓盐酸、95%乙醇、真空干燥;
方法二:(5)利用电解原理制备CuCl,阳极发生氧化反应,Cu失去电子,与氯离子作用生成CuCl,阳极的电极反应式为:Cu-e-+Cl-=CuCl,
故答案为:Cu-e-+Cl-=CuCl;
(6)虽然Ksp(CuCl)远远大于Ksp(CuOH),但阳极区Cl-浓度远远高于OH-的浓度,故开始没有CuOH生成,而是生成CuCl,
故答案为:阳极区Cl-浓度远远高于OH-的浓度.
点评 本题考查实验制备方案,涉及对工艺流程的理解、对操作与试剂的分析评价、平衡移动、电解原理、溶度积应用等,是对学生综合能力的考查,需要学生具备扎实的基础,难度中等.

| A. | 原混合溶液中c(Na+ )=6mol/L | B. | 电解后溶液中c(H+)=4mol/L | ||
| C. | 上述电解过程中共转移8mol电子 | D. | 电解后得到的Cu的物质的量为2mol |
| A. | 造成“酸雨”的罪魁祸首 | B. | 水溶液呈碱性 | ||
| C. | 可以是品红溶液褪色 | D. | 可以使澄清的石灰水变浑浊 |
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
 .
.(2)表中能形成两性氢氧化物的元素是铝(填元素名称),写出该元素的单质与⑨最高价氧化物的水化物反应的离子方程式2Al+2OH-+2H2O=2AlO2-+3H2↑.
(3)①、④、⑤、⑥、⑦、⑨六种元素的最高价氧化物的水化物中,按碱性减弱酸性增强的顺序排列为(用化学式表示)KOH、Mg(OH)2、Al(OH)3、H2CO3、H2SO4、HClO4.
(4)③元素与⑩元素两者核电荷数之差是26.
(5)请写出②的氢化物发生催化氧化的化学方程式4NH3+5O2
 4NO+6H2O.
4NO+6H2O. 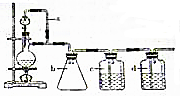 某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:CH2CH=CH2+CO+H2$→_{△}^{催化剂}$CH3CH3CH2CHO$→_{△}^{H_{2}催化剂}$CH3CH2CH2CH2OH.
某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:CH2CH=CH2+CO+H2$→_{△}^{催化剂}$CH3CH3CH2CHO$→_{△}^{H_{2}催化剂}$CH3CH2CH2CH2OH.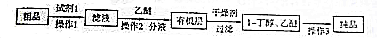
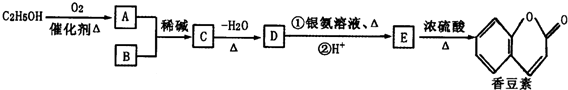
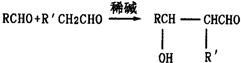 (R、R′为烃基或氢原子)
(R、R′为烃基或氢原子)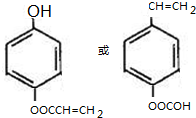 .
.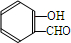 $\stackrel{NaOH}{→}$
$\stackrel{NaOH}{→}$ 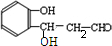 .
.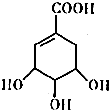 莽草酸的结构简式如图.请回答:
莽草酸的结构简式如图.请回答: