题目内容
右图表示反应2X(g) Y(g)+2Z(g),△H>0,在某温度时X的浓度随时间变
Y(g)+2Z(g),△H>0,在某温度时X的浓度随时间变
化曲线:下列说法正确的是

 Y(g)+2Z(g),△H>0,在某温度时X的浓度随时间变
Y(g)+2Z(g),△H>0,在某温度时X的浓度随时间变化曲线:下列说法正确的是

| A.2min时X的平均转化率为50% |
| B.第6min后,反应就停止了 |
| C.若升高温度,X的平衡转化率将减小 |
| D.若减小压强,v正和v逆将以同样倍数减小 |
A
根据图像可知,2mion时X的浓度是0.5mol/L,所以X的浓度变化量是1.0mol/L-0.5mol/L-0.5mol/L,因此X的转化率是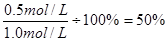 。6min后各种物质的浓度不再发生变化,说明反应达到了平衡状态,反应速率不等于0,反应并没有停止。正反应是吸热反应,所以升高温度平衡向正反应方向移动,X的转化率增大。因为反应前后体积是增大,所以降低压强,正逆反应均减小,但减小的倍数是逆反应速率大于正反应速率,所以平衡向正反应方向移动。答案选A。
。6min后各种物质的浓度不再发生变化,说明反应达到了平衡状态,反应速率不等于0,反应并没有停止。正反应是吸热反应,所以升高温度平衡向正反应方向移动,X的转化率增大。因为反应前后体积是增大,所以降低压强,正逆反应均减小,但减小的倍数是逆反应速率大于正反应速率,所以平衡向正反应方向移动。答案选A。
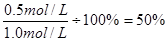 。6min后各种物质的浓度不再发生变化,说明反应达到了平衡状态,反应速率不等于0,反应并没有停止。正反应是吸热反应,所以升高温度平衡向正反应方向移动,X的转化率增大。因为反应前后体积是增大,所以降低压强,正逆反应均减小,但减小的倍数是逆反应速率大于正反应速率,所以平衡向正反应方向移动。答案选A。
。6min后各种物质的浓度不再发生变化,说明反应达到了平衡状态,反应速率不等于0,反应并没有停止。正反应是吸热反应,所以升高温度平衡向正反应方向移动,X的转化率增大。因为反应前后体积是增大,所以降低压强,正逆反应均减小,但减小的倍数是逆反应速率大于正反应速率,所以平衡向正反应方向移动。答案选A。
练习册系列答案
相关题目

 (1)2 min时,容器内n(N2)== ,c(H2)== 。
(1)2 min时,容器内n(N2)== ,c(H2)== 。
 (3)2 min时,容器内气体的总物质的量与反应前容器内气体的总物质的量之比为:
(3)2 min时,容器内气体的总物质的量与反应前容器内气体的总物质的量之比为: 2SO3 (g)若经过2s后测得SO3的浓度为0.6 mol/ L,试计算:
2SO3 (g)若经过2s后测得SO3的浓度为0.6 mol/ L,试计算: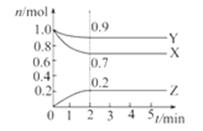
 2NH3(g) 反应,此反应达到化学平衡状态的标志是:①N2,H2和NH3的质量分数不再改变,②容器内的压强不随时间的变化而变化,③c(N2)∶c(H2)∶c(NH3)=1∶3∶2 ,④单位时间里每增加1molN2,同时增加3molH2,⑤一段时间内N2:H2:NH3的平均化学反应速率之比为1:3:2 ,⑥容器中气体的密度不变
2NH3(g) 反应,此反应达到化学平衡状态的标志是:①N2,H2和NH3的质量分数不再改变,②容器内的压强不随时间的变化而变化,③c(N2)∶c(H2)∶c(NH3)=1∶3∶2 ,④单位时间里每增加1molN2,同时增加3molH2,⑤一段时间内N2:H2:NH3的平均化学反应速率之比为1:3:2 ,⑥容器中气体的密度不变 NO+SO3,当反应达平衡时,下列叙述正确的时:
NO+SO3,当反应达平衡时,下列叙述正确的时: