题目内容
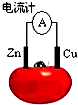 在番茄中将锌片和铜片按图所示方式插入,电流计的指针发生偏转.下列针对该装置的说法正确的是( )
在番茄中将锌片和铜片按图所示方式插入,电流计的指针发生偏转.下列针对该装置的说法正确的是( )分析:锌比铜活泼,锌为负极,发生氧化反应,电极方程式为Zn-2e-=Zn2+,铜为正极,发生还原反应,电极方程式为2H++2e-=H2↑,以此解答.
解答:解:该装置为原电池装置,能将化学能转化为电能,由于锌比铜活泼,则锌为负极,被氧化而腐蚀,铜为正极,电子由锌极经外电路流向铜极,
故选A.
故选A.
点评:本题考查原电池知识,侧重于学生的分析能力和基本概念的考查,为高频考点,有利于培养学生的良好科学元素,提高学习的积极性,难度不大,注意把握原电池的组成条件和工作原理.

练习册系列答案
相关题目