题目内容
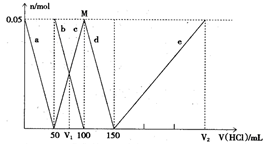
(6分)某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示,
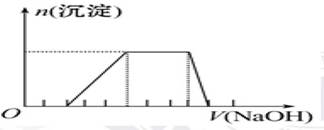
由此可知,该溶液中肯定含有的阳离子是_______________________,且各离子的物质的量之比为_____ ;肯定不含的阳离子是_____________ 。

由此可知,该溶液中肯定含有的阳离子是_______________________,且各离子的物质的量之比为_____ ;肯定不含的阳离子是_____________ 。
(6分)H+、Al3+、NH4+ 2∶1∶3 Mg2+、Fe3+
从图象可知,开始时无沉淀产生,说明含有H+,H++OH-=H2O,该氢离子消耗NaOH溶液的体积为2体积,图象中有一段平台,说明加入OH-时无沉淀生成,有NH4+,NH4++OH-=NH3?H2O,铵根消耗氢氧化钠为3体积,最后溶液中无沉淀,说明溶液中不含Mg2+和Fe3+,含有Al3+,根据Al3++3 OH-=Al(OH)3↓,铝离子消耗NaOH溶液的体积为3体积,当消耗4体积的氢氧化钠时沉淀消失,所以可得到H+、Al3+、NH4+的物质的量之比为2:1:3.
故答案为:H+、Al3+、NH4+;2:1:3;Mg2+、Fe3+.
点评:本题考查离子的判断和计算,题目难度中等,要求学生熟记物质的性质并灵活应用.
故答案为:H+、Al3+、NH4+;2:1:3;Mg2+、Fe3+.
点评:本题考查离子的判断和计算,题目难度中等,要求学生熟记物质的性质并灵活应用.

练习册系列答案
相关题目
 mL容量瓶④500mL容量瓶⑤玻璃棒⑥托盘天平(带砝码)配制时,必须使用的仪器有 (填序号),还缺少的仪器是 实验两次用到玻璃棒,其作用分别是 、 。
mL容量瓶④500mL容量瓶⑤玻璃棒⑥托盘天平(带砝码)配制时,必须使用的仪器有 (填序号),还缺少的仪器是 实验两次用到玻璃棒,其作用分别是 、 。 将实验③中的碱性溶液加热,有气体放出,该气体
将实验③中的碱性溶液加热,有气体放出,该气体 能使湿润的红色石蕊试纸变蓝。
能使湿润的红色石蕊试纸变蓝。