题目内容
 利用如图所示的装置,可以验证NH3和HCl的有关性质.实验前a、b、c活塞均关闭.
利用如图所示的装置,可以验证NH3和HCl的有关性质.实验前a、b、c活塞均关闭.
(1)若要在烧瓶Ⅱ中产生“喷泉”现象,烧瓶Ⅰ中不产生“喷泉”现象,其操作方法是______.
(2)若先打开a、c活塞,再挤压胶头滴管(假设NH?不被完全吸收),在烧瓶Ⅱ中可观察到的现象是______.
(3)通过挤压胶头滴管和控制活塞的开关,在烧瓶Ⅰ中产生“喷泉”现象,烧瓶Ⅱ中不产生“喷泉”现象,其操作方法是______.
解:(1)烧瓶Ⅱ中产生喷泉现象,烧瓶Ⅰ中不产生“喷泉”现象,利用氨气极易溶于水和装置中的压强关系,关闭c打开ab,挤压胶头滴管中的水,氨气溶于水烧瓶中压强减小,在外界大气压作用下水被压入烧瓶,气体溶解,压强减小,不断形成喷泉,
故答案为:关闭c打开ab,挤压胶头滴管中的水;
(2)挤压胶头滴管烧瓶Ⅱ中的氨气溶于水,使烧瓶Ⅱ中的气压减小,烧瓶Ⅰ中的氯化氢气体就会逸散到烧瓶Ⅱ中,与氨气反应产生白烟;可知烧瓶Ⅰ、烧瓶Ⅱ中的气压都减小,形成喷泉,故答案为:有白烟出现;
(3)在烧瓶Ⅰ中产生“喷泉”现象,烧瓶Ⅱ中不产生“喷泉”现象,需要先关闭b,打开ac,利用挤压胶头滴管中的水使烧瓶中的压强减小,烧瓶Ⅰ中的氯化氢气体就会逸散到烧瓶Ⅱ中,烧瓶Ⅰ、烧瓶Ⅱ中的气压都减小,再关闭c打开b,在外界大气压作用下在烧瓶中形成喷泉现象,
故答案为:关闭b,打开ac,挤压胶头滴管中的水,然后关闭a,打开b.
分析:(1)烧瓶Ⅱ中产生喷泉现象,烧瓶Ⅰ中不产生“喷泉”现象,利用氨气极易溶于水和装置中的压强关系分析判断;
(2)挤压胶头滴管烧瓶Ⅱ中的氨气溶于水,使烧瓶Ⅱ中的气压减小,烧瓶Ⅰ中的氯化氢气体就会逸散到烧瓶Ⅱ中,氯化氢与氨气反应产生白烟;
(3)在烧瓶Ⅰ中产生“喷泉”现象,烧瓶Ⅱ中不产生“喷泉”现象,需要先关闭b,打开ac,利用挤压胶头滴管中的水使烧瓶中的压强减小,烧瓶Ⅰ中的氯化氢气体就会逸散到烧瓶Ⅱ中,烧瓶Ⅰ、烧瓶Ⅱ中的气压都减小,再关闭c打开b.
点评:本题考查同学们接受信息、分析信息、根据信息解决问题的能力,解决这种类型的题目时,一定要分析题中所给的信息,如本题给了很多阀门,所以我们要充分利用这些阀门来解决问题.
故答案为:关闭c打开ab,挤压胶头滴管中的水;
(2)挤压胶头滴管烧瓶Ⅱ中的氨气溶于水,使烧瓶Ⅱ中的气压减小,烧瓶Ⅰ中的氯化氢气体就会逸散到烧瓶Ⅱ中,与氨气反应产生白烟;可知烧瓶Ⅰ、烧瓶Ⅱ中的气压都减小,形成喷泉,故答案为:有白烟出现;
(3)在烧瓶Ⅰ中产生“喷泉”现象,烧瓶Ⅱ中不产生“喷泉”现象,需要先关闭b,打开ac,利用挤压胶头滴管中的水使烧瓶中的压强减小,烧瓶Ⅰ中的氯化氢气体就会逸散到烧瓶Ⅱ中,烧瓶Ⅰ、烧瓶Ⅱ中的气压都减小,再关闭c打开b,在外界大气压作用下在烧瓶中形成喷泉现象,
故答案为:关闭b,打开ac,挤压胶头滴管中的水,然后关闭a,打开b.
分析:(1)烧瓶Ⅱ中产生喷泉现象,烧瓶Ⅰ中不产生“喷泉”现象,利用氨气极易溶于水和装置中的压强关系分析判断;
(2)挤压胶头滴管烧瓶Ⅱ中的氨气溶于水,使烧瓶Ⅱ中的气压减小,烧瓶Ⅰ中的氯化氢气体就会逸散到烧瓶Ⅱ中,氯化氢与氨气反应产生白烟;
(3)在烧瓶Ⅰ中产生“喷泉”现象,烧瓶Ⅱ中不产生“喷泉”现象,需要先关闭b,打开ac,利用挤压胶头滴管中的水使烧瓶中的压强减小,烧瓶Ⅰ中的氯化氢气体就会逸散到烧瓶Ⅱ中,烧瓶Ⅰ、烧瓶Ⅱ中的气压都减小,再关闭c打开b.
点评:本题考查同学们接受信息、分析信息、根据信息解决问题的能力,解决这种类型的题目时,一定要分析题中所给的信息,如本题给了很多阀门,所以我们要充分利用这些阀门来解决问题.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
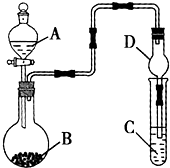 利用如图所示的装置进行实验,将液体A逐滴加入烧瓶中与B发生反应,下列有关叙述中不正确的是( )
利用如图所示的装置进行实验,将液体A逐滴加入烧瓶中与B发生反应,下列有关叙述中不正确的是( )| A、若A为硫酸,B为亚硫酸钠,C中盛品红溶液,则C中溶液褪色 | B、若A为醋酸,B为贝壳,C中盛澄清石灰水,则C中溶液变浑浊 | C、若A为浓氨水,B为生石灰,C中盛AgCl3溶液,则C中先产生沉淀后沉淀溶解 | D、仪器D可以起到防止溶液倒吸的作用 |

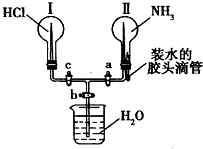 利用如图所示的装置,可以验证NH3和HCl的有关性质.实验前a、b、c活塞均关闭.
利用如图所示的装置,可以验证NH3和HCl的有关性质.实验前a、b、c活塞均关闭.