题目内容
7.下列关于氧化还原反应说法正确的是( )| A. | 一种元素被氧化,肯定有另外一种元素被还原 | |
| B. | 金属单质只有还原性,非金属单质只有氧化性 | |
| C. | 元素原子失电子数越多还原性越强,得电子数越多氧化性越强 | |
| D. | 有单质参加的化合反应和有单质生成的分解反应一定是氧化还原反应 |
分析 A.可能同种元素既被氧化也被还原;
B.非金属单质可得到电子,也可失去电子;
C.氧化性与得电子能力有关,得电子能力越强,则氧化性越强,与得电子多少无关,还原性与失电子能力有关;失电子能力越强,则还原性越强,与失电子多少无关;
D.有单质参加的化合反应和有单质生成的分解反应,一定有元素化合价的变化.
解答 解:A.可能同种元素既被氧化也被还原,如氯气与水的反应、氯气与NaOH的反应,故A错误;
B.非金属单质可得到电子,也可失去电子,如氯气与水反应,氯气既是氧化剂也是还原剂,而金属只能失去电子作还原剂,故B错误;
C.氧化性与得电子能力有关,得电子能力越强,则氧化性越强,与得电子多少无关;还原性与失电子能力有关,失电子能力越强,则还原性越强,与失电子多少无关,故C错误;
D.有单质参加的化合反应和有单质生成的分解反应,一定有元素化合价的变化,所以一定是氧化还原反应,故D正确;
故选D.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念的考查,注意利用实例来分析,题目难度不大.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
17.下列实验做法正确的是:
①用浓硝酸清洗做过银镜反应的试管;
②皮肤上粘有苯酚,立刻用酒精清洗;
③用稀硝酸洗涤乙醛和新制Cu(OH)2反应过的试管;
④用浓硫酸清洗盛过乙酸乙酯的试管.
关于他的操作( )
①用浓硝酸清洗做过银镜反应的试管;
②皮肤上粘有苯酚,立刻用酒精清洗;
③用稀硝酸洗涤乙醛和新制Cu(OH)2反应过的试管;
④用浓硫酸清洗盛过乙酸乙酯的试管.
关于他的操作( )
| A. | ①不对 | B. | ②不对 | C. | ③不对 | D. | ④不对 |
18.已知溶液中存在Cr2O72-+H2O?2CrO42-+2H+的平衡,其中Cr2O72-呈橙色,CrO42-呈黄色,向该平衡体系中滴加饱和NaOH溶液时,颜色的变化情况是( )
| A. | 黄色加深 | B. | 橙色加深 | C. | 颜色不变 | D. | 颜色褪去 |
15.下列叙述正确的是( )
| A. | 氧气的摩尔质量为32g | B. | NA个 O2分子的总质量为32g/mol | ||
| C. | 16g O2 的体积为11.2L | D. | 32g O2 的物质的量为1mol |
2.用NA表示阿伏德罗常数,下列叙述正确的是( )
| A. | 含有NA个CO和N2的混合气体,质量一定为28g | |
| B. | 将含0.01mol FeCl3的饱和溶液滴入沸水中,制得氢氧化铁胶体粒子数为0.01NA | |
| C. | 标准状况下,22.4L CCl4含有的原子数为5NA | |
| D. | 0.5mol•L-1的MgCl2溶液中,含有Cl-个数为NA |
16.分析用石灰水保存鲜蛋的原理如下:
(1)石灰水是碱性物质,能渗入蛋内和酸性物质反应,防止酸败;
(2)石灰水是电解质溶液,促使蛋白质凝聚;
(3)石灰水显弱碱性,有杀菌能力;
(4)石灰水能与鲜蛋呼出的CO2生成CaCO3薄膜,起保护作用.
其中正确的是( )
(1)石灰水是碱性物质,能渗入蛋内和酸性物质反应,防止酸败;
(2)石灰水是电解质溶液,促使蛋白质凝聚;
(3)石灰水显弱碱性,有杀菌能力;
(4)石灰水能与鲜蛋呼出的CO2生成CaCO3薄膜,起保护作用.
其中正确的是( )
| A. | (1)(2) | B. | (1)(2)(3) | C. | (3)(4) | D. | (2)(3)(4) |
13.某有机化合物D的结构为 ,是一种常见的有机溶剂,它可以通过下列三步反应制得:
,是一种常见的有机溶剂,它可以通过下列三步反应制得: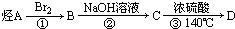 ,下列相关说法中正确的是( )
,下列相关说法中正确的是( )
 ,是一种常见的有机溶剂,它可以通过下列三步反应制得:
,是一种常见的有机溶剂,它可以通过下列三步反应制得: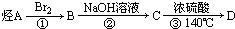 ,下列相关说法中正确的是( )
,下列相关说法中正确的是( )| A. | 烃A为CH3CH3 | B. | 反应②属于消去反应 | ||
| C. | 反应①②③都属于取代反应 | D. | 化合物D属于醚 |
