题目内容
1.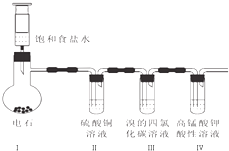 实验室制乙炔并检验其性质的装置如图.
实验室制乙炔并检验其性质的装置如图.(1)装置Ⅰ:发生的主要反应是CaC2+2H2O=Ca(OH)2+C2H2↑
(2)装置Ⅱ:由于电石中混有CaS、Ca3P2等,二者与水反应与装置Ⅰ中的反应类似.由此推断乙炔气体中混有硫化氢、磷化氢气体.装置Ⅱ的作用是吸收硫化氢气体,避免对乙炔的检验造成干扰
(3)装置Ⅲ:观察到的反应现象是溴水褪色,发生的反应方程式是CH≡CH+2Br2→CHBr2CHBr2(反应物物质的量1:1)
(4)装置Ⅳ:发生的反应类型是氧化反应.
分析 (1)电石与水反应生成乙炔;
(2)依据乙炔的反应原理得出混有的杂质气体时硫化氢和磷化氢,硫酸铜与硫化氢反应生成硫化铜沉淀;
(3)乙炔含有碳碳三键,能与溴水发生加成反应使其褪色;
(4)乙炔中含有碳碳三键,能被高锰酸钾溶液氧化,据此解答即可.
解答 解:(1)碳化钙(CaC2)与水反应生成氢氧化钙[Ca(OH)2]和乙炔,反应的化学方程式为:CaC2+2H2O=Ca(OH)2+C2H2↑,故答案为:CaC2+2H2O=Ca(OH)2+C2H2↑;
(2)CaS、Ca3P2与水反应生成硫化氢和磷化氢,此反应中会产生杂质气体硫化氢,会对乙炔性质实验造成干扰,利用硫酸铜溶液吸收硫化氢气体,故答案为:硫化氢、磷化氢;吸收硫化氢气体,避免对乙炔的检验造成干扰;
(3)乙炔还能够与溴发生加成反应,使溴的四氯化碳溶液褪色,该反应为加成反应,化学反应方程式为:CH≡CH+2Br2→CHBr2CHBr2,故答案为:溶液褪色;CH≡CH+2Br2→CHBr2CHBr2;
(4)乙炔分子中含有官能团碳碳三键,能够被酸性高锰酸钾溶液氧化,使酸性高锰酸钾溶液褪色,该反应为氧化反应,故答案为:氧化反应.
点评 本题主要考查的是乙炔的实验室制法以及乙炔的性质实验,涉及化学反应方程式书写、混合气体的除杂、有机化学反应类型的判断等,涉及知识点较多,但是难度不大.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
12.下列说法中正确的是( )
| A. | 硫酸分子中既存在一般的共价键,同时还有配位键 | |
| B. | 1个氮气分子中含有2个σ键和1个π键 | |
| C. | 能够用来衡量化学键强弱的物理量有:原子化热、晶格能、键能、氢键等 | |
| D. | NH4+中4个N-H键的键能不相同 |
16.下列化合物分子中,在核磁共振谱图中能给出4种信号的是( )
| A. | CH2=CH2 | B. | HCOOCH3 | C. | CH3COOCH2CH2CH3 | D. | CH3 CH2CH2CH3 |
6.下列结论是从某同学的作业本上摘录的,其中你认为肯定正确的是( )
①微粒半径:S2->Cl>S
②氢化物的稳定性:HF>HCl>H2S
③还原性:S2->Cl->Br-
④氧化性:Cl2>S>Se
⑤酸性:H2SO4>HClO4>H2SeO4
⑥得电子能力:F>Cl>S.
①微粒半径:S2->Cl>S
②氢化物的稳定性:HF>HCl>H2S
③还原性:S2->Cl->Br-
④氧化性:Cl2>S>Se
⑤酸性:H2SO4>HClO4>H2SeO4
⑥得电子能力:F>Cl>S.
| A. | ①⑤ | B. | ①③④ | C. | ②④⑥ | D. | ⑥ |
10.扑热息痛是一种解热镇痛药,结构式为 .下列说法中错误的是( )
.下列说法中错误的是( )
 .下列说法中错误的是( )
.下列说法中错误的是( )| A. | 扑热息痛的分子式为C8H9NO2 | |
| B. | 扑热息痛可与烧碱溶液、浓溴水溶液发生反应 | |
| C. | 扑热息痛很稳定,不容易被氧化 | |
| D. | 扑热息痛核磁共振氢谱上有5个峰,峰面积之比为1:1:2:2:3 |