题目内容
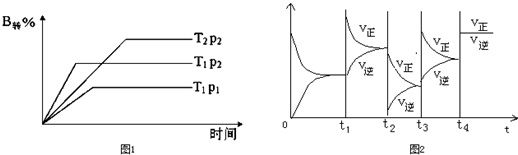
在密闭容器中,使2molN2和6molH2混合发生反应:N2(g)+3H2(g)?2NH3(g)(正反应为放热反应)下列说法错误的是( )
| A.升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量变大 |
| B.升高平衡体系的温度(保持体积不变),混合气体的密度不变 |
| C.当反应达到平衡时,N2和H2的浓度比是1:3 |
| D.当达到平衡时,充入氩气,并保持压强不变,平衡将逆向移动 |
A、混合气体的平均相对分子质量=
,反应前后质量守恒,升温平衡逆向进行,气体物质的量增大,混合气体的平均相对分子质量减小,故A错误;
B、混合气体密度=
,升温平衡移动,但气体质量不变,体积不变,混合气体密度不变,故B正确;
C、起始量1:3,反应比为1;3,所以得到平衡浓度1;3,故C正确;
D、恒温恒容容器,加入氩气,总压增大,保持压强不变,体积增大,平衡逆向进行,故D正确;
故选A.
| 气体质量 |
| 气体物质的量 |
B、混合气体密度=
| 气体质量 |
| 体积 |
C、起始量1:3,反应比为1;3,所以得到平衡浓度1;3,故C正确;
D、恒温恒容容器,加入氩气,总压增大,保持压强不变,体积增大,平衡逆向进行,故D正确;
故选A.

练习册系列答案
相关题目