题目内容
下列有关说法正确的是
A.25℃时,pH=5盐酸和pH=9的氨水,两溶液中水的电离程度不同
B.25℃时,Ksp(A)> Ksp(B),说明化合物A的溶解度比化合物B的大
C.常温下pH=4的盐酸中:c(H+)=c(OH-)+c(Cl-)
D.在NH4Cl溶液中加入适量硫酸,可使c(NH4+):c(Cl-)接近1:1
A.25℃时,pH=5盐酸和pH=9的氨水,两溶液中水的电离程度不同
B.25℃时,Ksp(A)> Ksp(B),说明化合物A的溶解度比化合物B的大
C.常温下pH=4的盐酸中:c(H+)=c(OH-)+c(Cl-)
D.在NH4Cl溶液中加入适量硫酸,可使c(NH4+):c(Cl-)接近1:1
CD
试题分析:由于盐酸是酸,而氨水是碱,故两者都是抑制水的电离,所以25℃时,pH=5盐酸和pH=9的氨水,两溶液中水的电离程度是相同的,故A错误;溶解度的大小与溶度积没有必然的联系,故.25℃时,Ksp(A)> Ksp(B),不能确定化合物A的溶解度比化合物B的大,故B错误;常温下pH=4的盐酸中,根据电荷守恒可以得到,c(H+)=c(OH-)+c(Cl-),故C正确;NH4Cl为强酸弱碱盐,其水溶液中由于铵根离子的水解而呈酸性,加入硫酸可以抑制其铵根离子的水解,所以加入适量硫酸,可使c(NH4+):c(Cl-)接近1:1,故D正确,所以本题的正确答案为CD。
点评:本题考查了强弱电解质、电荷守恒、盐类水解,这些考点均是高考考查的重点和难点,本题要理解的是酸和碱都能够抑制水的电离,无论是强酸还是弱酸,该题难度中等。

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
 Ag+(aq)+Cl-(aq)在水中的沉淀溶解平衡曲线如图所示。
Ag+(aq)+Cl-(aq)在水中的沉淀溶解平衡曲线如图所示。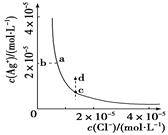

 2NH3(g) ;△H= —92.4 KJ·mol—1。现在500℃、20 MPa时,将N2、H2置于一个容积为2 L的密闭容器中发生反应,反应过程中各物质的物质的量变化如右图。回答下列问题:
2NH3(g) ;△H= —92.4 KJ·mol—1。现在500℃、20 MPa时,将N2、H2置于一个容积为2 L的密闭容器中发生反应,反应过程中各物质的物质的量变化如右图。回答下列问题: