题目内容
硼有两种天然同位素10B和11B,硼元素的相对原子质量为10.8,则10B与11B的物质的量之比为( )
| A.1∶4 | B.1∶2 | C.1∶1 | D.1∶3 |
A
解析试题分析:假设10B与11B的物质的量之比为x:y.则硼元素的相对原子质量为(10x+11y) ÷(x+y)=10.8整理可得x:y=1:4.因此正确选项为A。
考点:考查硼元素的相对原子质量与同位素原子的关系的知识。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
有X、Y两种元素,原子序数≤20,X的原子半径小于Y,且X、Y原子的最外层电子数相
同(选项中m、n均为正整数)。下列说法正确的是( )
| A.若X(OH)n为强碱,则Y(OH)n也一定为强碱 |
| B.若HnXOm为强酸,则X的氢化物溶于水一定显酸性 |
| C.若X元素形成的单质是X2,则Y元素形成的单质一定是Y2 |
| D.若Y的最高正价为+ m,则X的最高正价一定为+ m |
下列有关化学用语使用正确的是( )
A.硫原子的原子结构示意图: |
B.NH4Cl的电子式: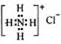 |
C.原子核内有10个中子的氧原子: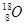 |
| D.纯碱的化学式为NaOH |
已知1~18号元素的离子aW3+、bX+、cY2—、dZ—都具有相同的电子层结构,下列关系正确的是( )
| A.质子数:c>d | B.离子的还原性:Y2—>Z — |
| C.氢化物的稳定性:H2Y>HZ | D.原子半径:X<W |
元素X的最高正价和负价的绝对值之差为6,元素Y原子次外层与元素X原子次外层均为8个电子,X、Y的离子具有相同的电子排布,X、Y形成的化合物是( )
| A.MgF2 | B.MgCl2 | C.CaCl2 | D.CaBr2 |
W、X、Y、Z是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,己是由Y元素形成的单质,常温下丙和己均为气体。已知反应:甲+乙 丁+己,甲+丙
丁+己,甲+丙 戊+己;常温下0.01 mol·L-1丁溶液的pH为12。下列说法正确的是
戊+己;常温下0.01 mol·L-1丁溶液的pH为12。下列说法正确的是
| A.元素X在周期表中的位置为第2周期ⅥA族 |
| B.元素X、Y、Z的原子半径由大到小的顺序为r(Z)>r(Y)>r(X) |
| C.1 mol甲与足量的乙完全反应转移的电子数为6.02×1023 |
| D.1.0 L0.1 mol·L-1戊溶液中阴离子的总物质的量小于0.1 mol |
甲、乙两种非金属性质比较:
①甲的单质熔、沸点比乙的低;
②甲单质能氧化乙原子的阴离子;
③最高价氧化物对应的水化物酸性比较,甲比乙的强;
④与金属反应时甲原子得电子的数目比乙多;
⑤甲单质比乙单质容易与氢气化合。
上述项目中能够说明甲比乙的非金属性强的是
| A.①②⑤ | B.③④⑤ | C.②③⑤ | D.②③④⑤ |
已知X为第三周期元素的原子,该原子要达到8电子稳定结构,则需要的电子数小于其次外层和最内层的电子数之差,且等于最内层电子数的整数倍。下列说法正确的是( )
| A.X元素最高价氧化物对应的水化物一定是强酸 |
| B.X元素的氢化物的化学式一定为H2X |
| C.X的单质一定是良好的半导体材料 |
| D.X元素的氧化物一定能与烧碱反应 |